��K���R����ʹ����V���Ŀ���ˎ֮һ��Ȼ������������K�a����ˎ�ԣ�ʹ��K�į�Ч�������͡���Q�[������ˎ�����������Y���P�I���}֮һ��������K��ˎ��ʧ��C�ư���1�������Ⱥ��w������ˎ��IJ��@��2�������Ⱥ����������ģ�GSH��������ף�MT���ȣ�����K�ĽY�ϡ�3������Ĥ�ϵ����ű��ų�ˎ�4��DNA�ޏ͙C�����������ء��^ȥ������wϵ�ѽ��܉��Qһ�N��Nʧ��C����ɵ���ˎ������Ҫ�˷����Ե��@Щ��ˎ�C��߀�dz����y��
�пƴ��˼���{���������d���Լ����R�ո߷������ĵĺ����߂�ᘌ���K��ˎ�ԵĶ�N�C�ƣ��OӋ���K(��)/�(��)�p���ٸ߷��ӿ���ԇ�����������D�[������K��ˎ�ԡ�ԓ�ɹ��ԡ�Fighting against drug-resistant tumors using a dual-responsive Pt(IV)/Ru(II) bimetallic polymer�����}Ŀ�l����Advanced Materials�ϡ���˼���������d���о��T��ԓՓ�ĵ�ͨӍ���ߡ�
�ڱ������У����߲����ăr�K�K�������w�c��������w�l���c���ۺϺϳ�ԓ�K(��)/�(��)�p���ٸ߷��ӡ������ֱ��ʹ����K���ăr�Kǰˎ�и����Ļ��W���ԣ��ɱ�����Ⱥ�����ĽY�϶������Kˎʧ�ͬ�r�ăr�Kǰˎ�ڼ�����߀ԭ�h���¿���ጷ���Kԭˎ�����⣬�Kˎ�cᑿ���ԇ������ʹ�����fͬ���á��ڼt�⣨671 nm�������£��ۺ����к�ᑲ������Mһ���a���ξ��B����������ˎ�[��������ᑿ���ԇ���Լ��ξ��B����������DNA�ēp����ͬ����K���µēp�����@Ҳ���Է�ֹ��DNA�ޏͶ��a������ˎ�����⣬ԓ�p���پۺ������ͨ�^�ԽM�b�γ�PolyPt/Ru�{�����ӣ�������PEG�ӿ��Ԝp�ٷ��خ��Ե������������LѪҺѭ�h�r�g�����C�����[����λ�ĸ������@�N�K(��)/�(��)�p���پۺ���ᘌ������Ķ�N��K��ˎ�C�ƣ��܉���Ч�Ŀ˷��[������ˎ�ԡ�
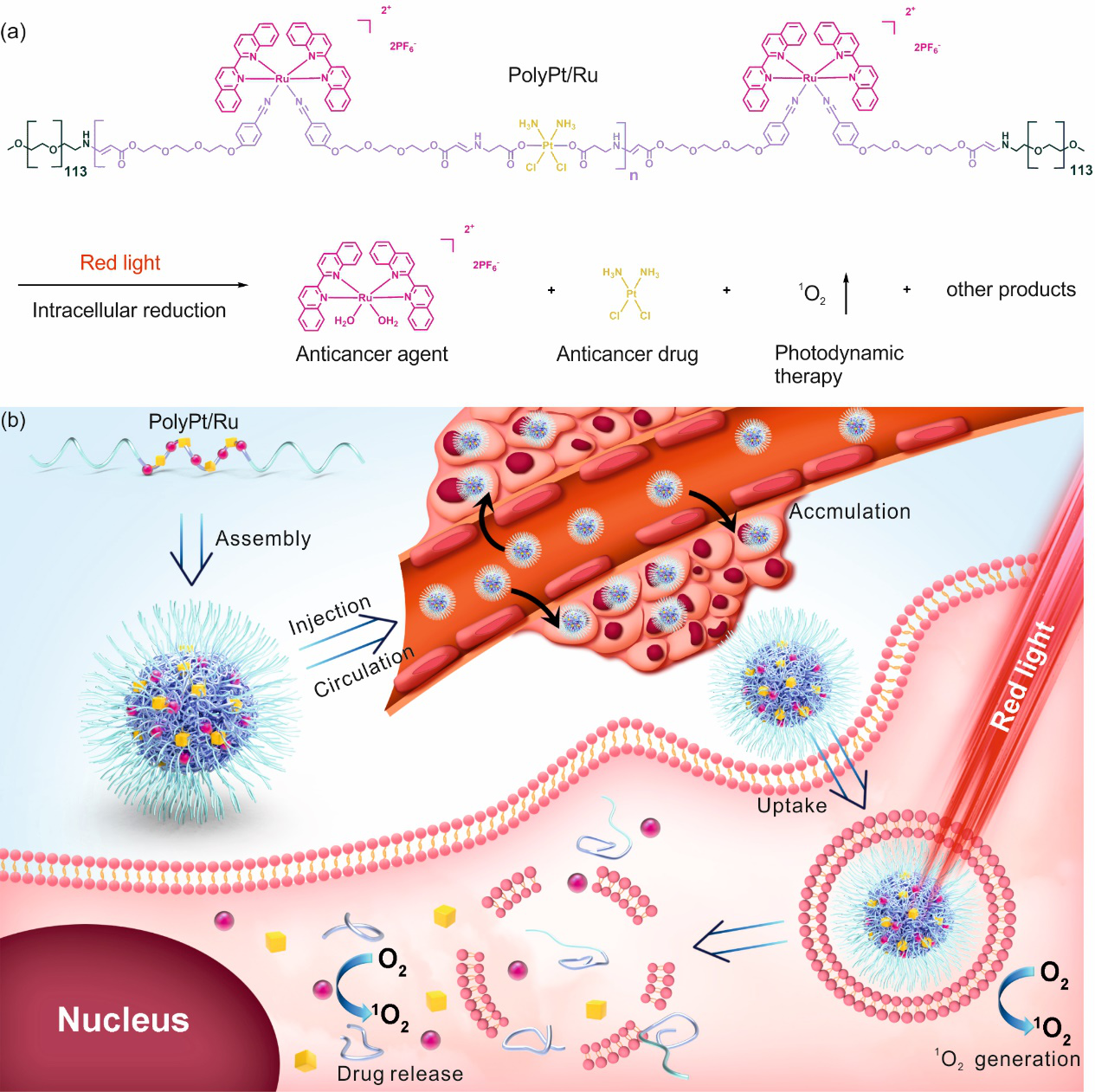
�D1.��a��PolyPt/Ru�Ļ��W�Y�����t��������Ɖ�PolyPt/Ru�ĽY��ጷ�Ru(II)����ﲢ�a���ξ��B��������GSH���Ɖ�PolyPt/Ru�ĽY����ጷſ���ˎ����K����b��ʹ��PolyPt/Ru���D��ˎ���[�����ۺ����ԽM�b��������ͼ����������^�̵�ʾ��D��Adapted under the terms and conditions of CC-BY (Adv. Mater. 2020, 2004766).
�о��߂����Ȍ��Ƃ���K(��)/�(��)�p���پۺ���{�������M���˻��W�Y���ı����Լ��w��ģ�M���ȭh��푑��Խ���Ĝyԇ���D2����

�D2.��a��PolyPt/Ru�{�����ӵ�TEM����b��PolyPt/Ru�{�����ӵ�DLS����c��PolyPt/Ru�{�����ӷքe�ڼt�������º�GSH̎���µ�DLS����d��PolyPt/Ru�քe�ڼt�������º�GSH̎���µ�GPC����e���t�������Ru���w���������չ��V����f���t�������Ru���w���ѽ��HPLC����g���t�������Ru���w���ѽ��ʾ��D����h��GSH̎����Pt���w�ѽ��ʾ��D����i��GSH̎����Pt���w�ѽ��195Pt�˴Ź���Adapted under the terms and conditions of CC-BY (Adv. Mater. 2020, 2004766).
�����Mһ���о���ԓ�{�����ӌ���K��ˎ���������L������Ч�����{�������ܱ���ˎ������Ч�zȡ���ڰ���߀ԭ�h���£���K���ԏļ{��������ጷš�ͬ�r�ڼt�⣨671 nm�������£�������Ҳ���ԏļ{��������ጷţ����a���ξ��B�����@�N�fͬ���ÿ��Դ����ߌ���ˎ������Ě������Ķ����D��K��ˎ���D3����

�D3. PolyPt/Ru�{�������ڣ�a��A549-DDP�ͣ�b��7404-CP20�����еļ����zȡ�О顣PolyPt/Ru�{�����ӌ���c��A549-DDP�ͣ�d��7404-CP20�ļ������ԡ����l����PolyPt/Ru�{�������ڣ�e��A549-DDP�ͣ�f��7404-CP20�����Іξ��B���ęz�y��Adapted under the terms and conditions of CC-BY (Adv. Mater. 2020, 2004766).
����ԓ�{�����Ӿ������õ��w�⿹�[��Ч���������Mһ��ͨ�^��Դ�[�����N��ֲ��PDX��ģ���C���������w�ȵ�����Ч����PDXģ���ڽM������W����������W�ͻ���ˮƽ�ϱ����˴ֲ���ԭ���[�������c�����кܺõ��R����Ч�A�y�ԡ��о��l�F��PolyPt/Ru�{�����ӿ��Ը�����PDX�[����λ���ڼt��������䌦�[�����LҲ�����@������Ч�����D4����

�D4.��a��PolyPt/Ru�{��������PDXģ��С���[����λ�ĸ�������b���t������С���[����λʾ��D����c��PolyPt/Ru�{�����ӌ��[�����L��������������d����ͬ�oˎ̎��������ء���e����ͬ�oˎ̎�����[�������߽M�����W������Adapted under the terms and conditions of CC-BY (Adv. Mater. 2020, 2004766).
������֮���@ƪ�о������y���������Ļ��W�����Լ�������ί���һ�w���״Έ���˻���푑��Ͷ������λ�ۺ����������D�[������K��ˎ�������ɞ�һ�N������[���ί����ԣ�����{���t�W�ṩ���µ��о�����
ԭ��朽ӣ�
https://onlinelibrary.wiley.com/doi/epdf/10.1002/adma.202004766
https://onlinelibrary.wiley.com/doi/10.1002/adma.202004766
https://doi.org/10.1002/adma.202004766
- ����������W��÷ؑ����/�ܾ������ڈF� AFM: ��푑���ˮ���zͨ�^ˮ�_�P�{��ģ�����ڼ������\�{�� 2025-12-13
- ����ҷ��ڽ��ڈF� AFM���o�܄��錧�ğ����Ծ۰����ͺϲ���-���з���������ğ�ɹ�푑� 2025-12-05
- �|���r����F� Small�������~���l�Ą��ȿ��{������ճ���� - ���ڿ՚⼰ˮ�²�ƽ�������ճ�� 2025-09-02
- �������S���e���ڈF� ACS Sensors����ϸ߷������z�˹�Ƥ�w�c������Ĥ�Ŀɴ���SERSоƬ �� ���F��Һ�������Y��־��o���z�y 2026-03-27
- ���Ї���AI+�²��ϡ���� - ��AI+�߷��Ӳ��ϡ���Փ�� Ͷ�����쵹Ӌ�r 2026-03-25
- �пƴ�������/���/�Y��F� Science��ϵ�y��ʾ�߷����d�w���ϰl��ϵ�y������ĵәC�� 2026-03-20
- �ϴ�����x/��� Angew.�����ͽ��پۺ���늽��|����������̑B䇽���늳����ܵ���ͻ�� 2024-12-06
