
���g����Ŀǰ���w���ί�����õķ���֮һ�����ڸ�Ⱦ���g���[���Ͱl�nj��w�����g�ί����R�ăɴ��������o���ί����g���o���ί��ڸ��ƻ����A����l�]��Ҫ���á���ˣ��_�l�µĸ�Ч�����g�o���ί����Կ˷������y�}��ʹ���ߵ��R���@������Ƿdz������x�ġ��{���g���N�²��ϵij��F���_�l����o�����ί��²����ṩ������ܡ����磬��ᯟ��(PTT)���J����һ�N��Ч���[���ί���������Ч��PTTͨ����Ҫ���и߹���D���ʺ��������������ԵĹ�ᄩ(PTAs)�����⣬푑���ጷ��dˎƽ�_���Ԍ��Fˎ�ﰴ���ጣ�Ҳ��һ�N����ǰ�������g�o�����ί����ԡ���PTT�{�ײ��ϵĺ�ˎ���f��ƽ�_�У����S��Ԫ�ز��ϣ�2D Xenes��(��ʯīϩ�����ס��Rϩ��) �����䪚�ص��������W���|�����J����PTAs���������֮һ���䪚�ص�������״��x����������������ڶ���OӋ�����a�͝��ڵ��R���D�������⣬���г��߱����w�e�ȵļ{��Ƭ(NS) 2D Xenes���Ԍ��F���dˎ���ܣ��o���Mһ����;���PTT��ˎ��ؓ�d�ɷN���ܡ�
��ǰ���C���Nϩ�����c(Ge QDs)��һ�N��Ч�Ĺ�Ό�[���{�ײ��ϣ�Angew Chem Int Ed Engl. 2019, 58(38):13405-13410����ֵ��һ����ǣ��N�������w��Ԫ�أ������w�����������{������l�]����Ҫ���ã��������õ����������Ժ͝��ڵ��t�W�rֵ������Ӌ��ÿ���ʳ���Дzȡ���NԪ�ش�s��367-3700���ˣ����N������������ʳ�a�䄩�к��Lһ�Κvʷ(ÿ��Ą������_1��)��һЩ���N����Ҫ�ɷֵ�ˎ��Ҳ�����������ί���ͬ�ļ��������[�����P���ס���ˣ��@Щ���صă����@���_�l����2D Ge�{��ˎ������ﰲȫ�Ժ͝��ڵ��t�Ãrֵ�����ǣ�Ŀǰ������ǰ��2D Ge��PTT�����о��⣬�r�������t�W���õĈ����2D Ge�{��ˎ��������t�W�����д������ھ�
���գ����ݎ�����Wˎ�WԺ�x����ڈF��c�����W�t�WԺ����Ԫ�о��T���Ղ����ڈF������۽��[�����g�ί������R�ďͰl��Ⱦ�ɴ�����ͻ���l���˶��S�Nϩ�{��Ƭ��Ge NSs�����[�����g�o���ί��еĝ���������Cell���s־��ÿ���Matter����������������Ϸ���피�����ϰl�����}�飺��Germanene-Based Theranostic Materials for Surgical Adjuvant Treatment: Inhibiting Tumor Recurrence and Wound Infection�������¡�ԓ�о������ؓ�d�R�����û���ˎ���簢ù�ء�����ϩ���Ķ��S�Nϩ�{��Ƭˮ���z����Ϳ�����ڌ��w�����g�o���ί����l�]�����[���Ͱl���A�����ڸ�Ⱦ���p�����á�ԓ����ͬ�r���x�顶Matter���s־���·���������https://www.cell.com/matter/fulltext/S2590-2385(20)30193-4�������ܵ��n���ƌWԺԺʿJong Seung Kim���ڈF꠵Č��}�ƽ�͈����https://www.cell.com/matter/fulltext/S2590-2385(20)30294-0������Matter���s־��Ĺٷ�������]��x��https://twitter.com/Matter_CP/status/1278344973402939392����

�n���ƌWԺԺʿJong Seung Kim���ڈF꠵Č��}�ƽ�͈��

��Matter���s־��Ĺٷ�������]
�@��о��У������״��ṩ�˻����Nϩ�{�ױ�Ƭ��Ge NSs���Č��w�[�����g�o���ί�ϵ�y:(i)��ģ�B����������ȫ���oˎ�l�]�gǰ���o���ί����ܣ�(ii)�����Nϩ��ˮ���z���F�g��ԭλ�ί��[���Ͱl�����Ƃ��ڸ�Ⱦ�������Ge�{��Ƭ��NSs�����F�����dˎ������푑���pH�ͽ��t��[NIR]���У�����ˎ��ጷ��О飬NIR�|�l����[���B���ܣ����õ������������Լ���ģʽ�����������[�����o���ί��ĝ��������cˮ���z����FDA���ʵĭ�֬�Ǻ͚����ǽM�ɣ��Y�Ϻ������dˎGe��ˮ���zͿ���[���g����ڱ��棬ͨ�^NIR���䣬�l�]�ֲ��ᯟ��NIR�|�l�Ļ���ˎ��ጷŵ����ã�һ�����܉���ٚ��皈���[�������ͼ�������һ����־ÿ��[�����־������ق������ϡ�
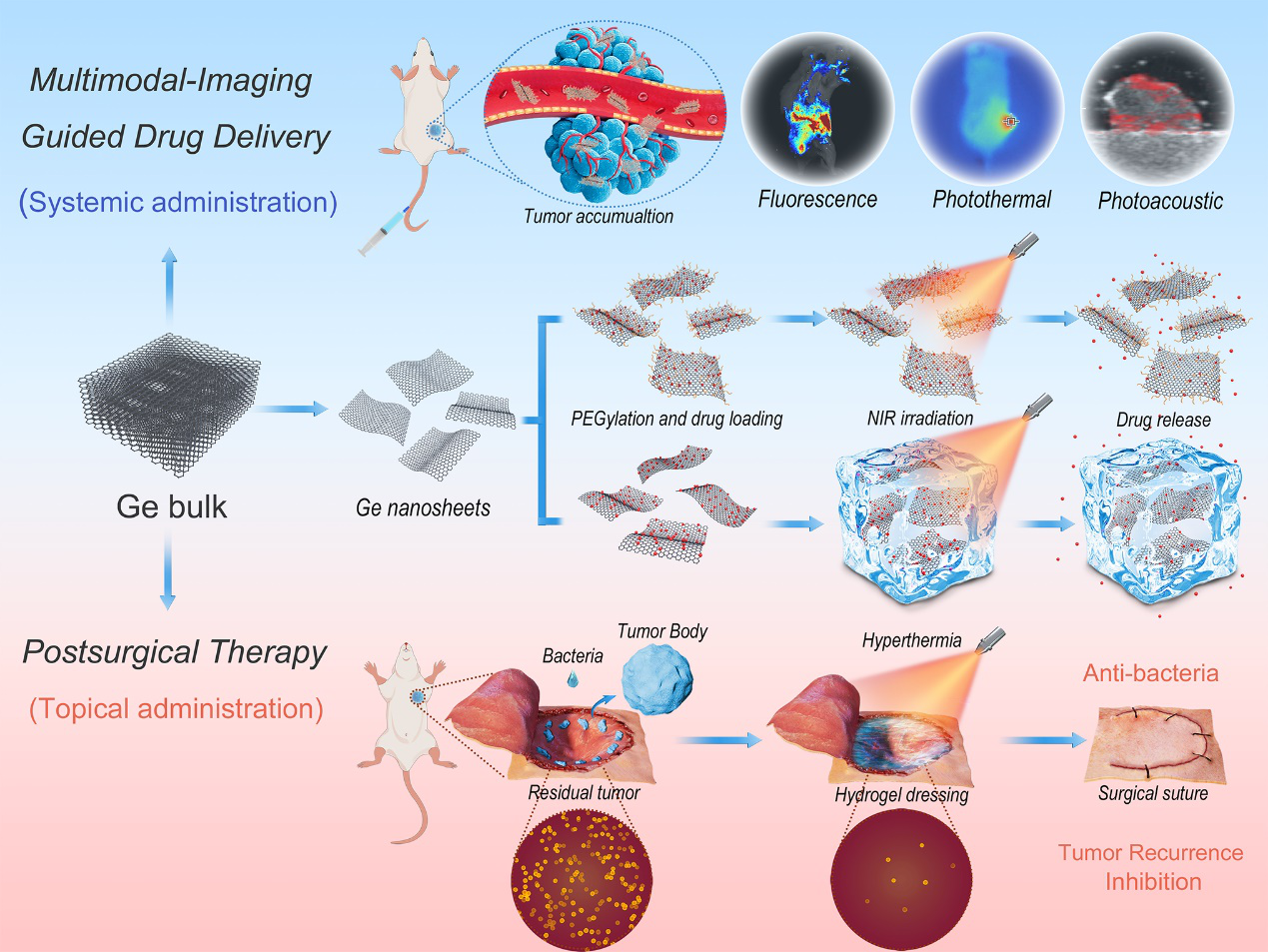
ʾ��D1. 2D Ge NSs����ˎ���f��ƽ�_���cˮ���z�Y�������[�����g�o���ί��������[���Ͱl�͂��ڸ�Ⱦ
���Y�����棬Ge NSs��Ge��ĩͨ�^��������϶��µ�Һ�����x���Ƃ䣬�Mһ����PEG���ؓ�d���[��ˎ�Ȼ��ͨ�^ԭ�����@�R��AFM����������@�R��TEM����X�侀��������V��XPS�����������V�M���˱���������߀��C�˲��ϵ�NIR�Լ�pH푑���ጷ����ܡ��Y���@ʾNIR�����52С�r��pH 5.0���� ����ˎ����ӵ��۷eጷ�������������97����

�D1. ����2D Ge��ˎ���f��ƽ�_�ı���
������C�����o���ί��đ��Ý��ܣ������Mһ���u����ˎ���f��ƽ�_���w����w�����ԡ�
�ڲ�ͬ����ϵ��Ѫ�����У�PEG @ Ge NSs ���F���������������ԡ���������ˎ��ጷŌ��Y�������w��3D�[��������ģ�����dˎPEG @ Ge NSs ���C������NIR�|�l����[���B���ܣ�NIR̎�����[�����ⲿ���Ȳ������ģ����^�쵽���@��ˎ��ɹ⣬���ڶ����Y���б��Mһ���C�������w�⿹�[��Ч���u���У����t���������dˎPEG @ Ge NSs�M�Ȍ��սM���F�����@���Ŀ��[��Ч�������ƵĽY���ڻ���Ⱦɫ����б�����ֱ�^���^�쵽�����⣬����߀�Ͳ��ό������wĤ�λ��Ӱ��M�����о���
���w���u������У��dˎPEG@Ge NSs���и��õ�ˎ�������W������Ȼ�����ߌ��dˎPEG@Ge NSs��ģʽ���ɹ�������������������ί��������M�����о����Y���@ʾ���o�}ע��4 h�����܉����[����λ�e�ۣ���ע��8 h�r��̖�@�����ӣ����c�����M�����@�^�e���f��PEG@Ge NSs�܉�ͨ�^ѪҺѭ�h���F���[���M���еķֲ���������ϵ�y�Ե��[�����o���ί������⣬����߀�Mһ����C��PEG@Ge NSs���õ��w�����������Ժ����ﰲȫ�ԡ�

�D2. ����Ge��ˎ���f��ƽ�_���w������

�D3. ����Ge��ˎ���f��ƽ�_���w������
���ˑ������[���g��ֲ��o���ί������ߌ�ؓ�d����ˎ���Ge NS�c���К����Ǻ͵����c��֬�ǵ�ˮ���z����Ƴɼ{��Ƭ�dˎˮ���zƽ�_�����Mһ�������z����ò��NIR�̼�푑���ˎ��ጷ������M�����u���������Mһ���u���{��Ƭ�dˎˮ���z���g���o���ί��Ќ��[���Ͱl���������ã����ߘ�����ԭλ����֬���|�[��ģ�ͣ��M���g���o���ί�Ч���u�����Y���@ʾ�{��Ƭ�dˎˮ���z���g��ֲ��o���ί��о����@�������[���Ͱl���á�

�D4. �dˎGe ˮ���z���g���o���ί��������[���Ͱl
���]�����ڼ�����Ⱦ�dz�Ҋ���g�l�Y֮һ�������Mһ����C�˼{��Ƭ�dˎˮ���z�Ŀ���Ч���ͼ��ق������ϵĝ��ܡ����Sɫ������������m����ԣ��ʹ��c�U�������m����ԣ����Á��u�����z�Ĺ��V�����ԡ��֞����M��G1�����սM��G2��hydrogel��G3��DOX @hydrogel��G4��Ge @hydrogel��G5��Ge @hydrogel+ NIR����G6��Ge/DOX@hydrogel+ NIR������Ge�ļ��r��ᚢ�������c�����ǵ��LЧ�־����ØO�õĽY�ϣ����G5��G6�M���F����100���Ě����־����á������Mһ���о����w���g���Ⱦ�Ŀ������ã����ߘ�����С����ڸ�Ⱦģ�ͣ����^���˲�ͬ̎���M��G1-G6���Ă����]�Ϻͼ���������r���Y���@ʾ��ˮ���z�ί��M�Ą������@�Ȍ��սM���ϸ��죺G5��G6�Ă��������g��12��Ȏ���ȫ���ϣ������սM�Ă�����e�Լs��ԭʼ���ڵ�16.7����4.1������ˮ���z̎���M�аl�F����ľ������ܽY������ѿ�M�������ڌ��սM���^�쵽����ĉ����M�����^�ٵ���ѿ�M������G2-G6�M�аl�F������G1�M�ٵöࣺ��������Ge @hydroge��ɫ�Ŀ���Ч������ G5��G6�л����z�y����������

�D5. Ge @hydrogel���@������Ч���ͼ��ٵĂ������ϝ���
���w���f�������ṩ�˻���Ge NSs���[�����g�o���ί����Ե�ԭ���C���������Ge NSs��������ˎ���f��ƽ�_�M���_�l���cˮ���z�Y��ʹ�Õr������Ϳ�����[���г��g��Ă��ڱ����ϣ��l�]�@���Ě����[�������������Լ����M�������ϝ��ܡ���ˣ����о����H�״Ό�2D Ge�����ڌ��w�[������o���ί�������߀���ܹĄ���ͬ�Ļ���2D Ge�������t�W������δ���������о������µĵ�һ�����ǹ����W�t�WԺ�{���t�W���������B��ʿ���T�����{���t�W���ĵ��Wꖽ���ʿ�����о�Ҳ��������Ҫؕ�I��
Փ��朽ӣ�https://www.cell.com/matter/fulltext/S2590-2385(20)30193-4
- �����ֿƴ��䏩/�ǫI�¡�����������ꐝ�/Ф�i��Nat. Commun.��: �nj��Q�H��ˮ���|�Y���ӿ���ˮ�Uɢ - �s��ˮ���z���F��Ч���ˮ�ռ� 2026-04-02
- ����i Adv. Mater.����x��-�л��i�Y����ע�䌧�ˮ���z - ���������ĽM��-������Ә��� 2026-03-21
- �Ͼ���W����/��� AFM�����ڸ�Ч�������l��s�ķ������w�����������ˮ���z 2026-03-20
- �пƴ�������/���/�Y��F� Science��ϵ�y��ʾ�߷����d�w���ϰl��ϵ�y������ĵәC�� 2026-03-20
- �㽭��W�������ڡ�����ܽ��ڈF� JCIS�����ڰ�ȫ�Ź������ʹ̼�푑�ˎ���f�͵ļ{������ 2025-09-09
- �|�ϴ�W�����۽����c������ Research�����ݞ�ģ��������Խ��ٶ���z������ˎ���f�ͺ��������[�������ί� 2025-07-31
- ��������ǵ��ΈF� ACS Nano�����Ӷ���@�o����λ�ۺ���ͺϼ{�������F�[���B�m�ߏ��ȹ��-���������ѭ�h�ί��ͻ��� 2025-08-01
