�����[���������{��������������[���fͬ�ί�������N�ί��ֶ�������������Ч���p�ٶ������á����У�����ί����������ί����������fͬ���Ԙ����������fͬ�M�ϡ�����ί�ͨ�^�ֲ��ӟ�Ѹ�ٚ����[�����������ί��r�g�̣�5-20��犣����L���ί�����ɾֲ��^����Ɖ������M�����������������û����������[���������ί��r�g�ɾS����С�r�������m�V�V��Ч���������^��������20С�r���������_����Чˎ���ί���������^�m�S��20-48С�r����ˣ������fͬ�ί����Կ���ʹ��N�����ă��ݻ��a���ѳɞ��[���fͬ�ί�����Ҫ�о�������Ȼ�����������������R�ɴ�����һ�ǹ���ί������ڽ��t���\���ӟ������������[���y�ԏص���������ڱ����^��ͽM���p����24С�r�ȟo���ٴ��ί������Ƕ�N�ί��ֶ��S�r�g�������y�ԅf�{�����εį����B�Ӻͽ��ʽ���ί�����/�����O����������ί��g϶�������ί������S�r�g�������ʽ�����ӣ�ʹ�[�������������������������w��Ч���ί�������ˎ���Ȳ��H���^�����M��߀����Ɍ������M���Ķ������ã����ܳ�ְl�]����ί����������ί��������ąfͬ�ί����ݡ���Q�������}���_�l������������Ĺ⯟�O�������_�����������ˎ�f��ϵ�y���_����ģ�B�fͬ�����ڏ��Ⱥ͕r�������f�{�yһ��
���ڣ�������ͨ��W�����WԺ�ǵ��ν��ڈF��аl�˹⯟ᘣ�PMN��ϵ�y������������˴���ȣ����F���B�m�⯟�������һ�N�B�m�ߏ��ȹ��-���������ѭ�h�ί����������[���fͬ�ί��²��ԡ�ԓ�������[������������������^�ͽyһ���ί��ֶΏ��ȵĘ˜ʣ������T����90%���������Ĺ��ضȡ����ɻ�����c�����������x��ߏ����ί��ֵ�����ڴˣ�������һ�����m48С�r�ߏ��ȅfͬ�ί����ԣ�ǰ20С�r���M��3�ι���ί���ÿ��10��犣������g�����������a�����ɻ������F���-����������ί���20С�r����ˎ�����_�ߏ����ֵ���M���L�_28С�r�ij��m�pˎ�����A�Σ��Ķ����F��48С�r�B�m�ߏ��ȵĿ��[���ί����D1�����_���˸�Ч���̈́����͵��������[���C���ί�Ч����

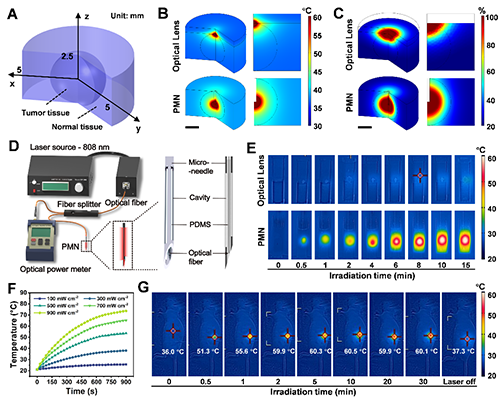
�D1. �[���B�m�ߏ��ȹ��-���������ѭ�h�ί�����������ʾ��D��(A)�ͺϼ{����Dp825:ARS@PDA-Fe(III)-FA ICP NCPs�Ƃ䣻(B) PMN�c��W�R���ܱ��^��(C)����^�ͽyһ���ί��ֶΏ��Ƚ������[�����������ʞ�˜ʵĺ����Pϵ��(D)���m�ߏ��ȹ��-����������ί����������g�ͺϼ{�������[��������׃����
�錍�Fԓ���ԣ��о��F��OӋ��һ�N�⯟ᘣ�PMN��ϵ�y�������w���^��ײ��P����ʹ����ͨ�^�ֱ�ӵ��_�[���M����ԓϵ�y�Ɍ��������ʂ������[�����������͌��܇������M���ğ�p���L�U��֧�ָ��L�r�g�Ͷ����ڵĹ��-������fͬ�ί���������PMN�Ĵ�����ǂ��y�R��20�����H��1/5�ļ���ʼ����_����ͬ�ί��ضȣ�������30��犃ȾS�֜��ȷ������@ʾ�����õĿɿ����c�����������D2�����˷��ˬF�й⯟ϵ�y�����y��
�D2. �⯟ᘣ�PMN���ķ���͌����C��(A)�p���[���M��ģ�ͣ�(B)��W�R��PMN������[���M���ضȷֲ���(C)��W�R��PMN������[���M����p����(D) PMNϵ�y�Y��ʾ��D��(E)��W�R��PMN�������z�ļt�����D��(F) PMN�������z�ض�׃����(G)PMN����С���[����λ�ļt�����D��
���⣬�F��OӋ��һ�N�p�ӏͺϼ{������Dp825:ARS@PDA-Fe(��)-FA ICP NCPs���s����NCPs�������}�ᰢù�أ�DOX����ᄩIR825ͨ�^���Ӷ����γɺ��ļ{������Dp825 NPs������Ӱ����Ծ۶�Ͱ���PDA����Fe(III)�x�Ӽ��~�ᣨFA�������ğo����λ�ۺ��ICP����ͬ�rؓ�d�������/����������������ARS����ԓNCPs�����[�������ԣ����ICP�����[���h�������ԭh��푑��ֽ⣬����ጷŸ��ί�������ɹ��-����������ί��������mጷŻ���ˎ���PMN�o�������F48С�r���B�m�ߏ����ί����_���˶�ģ�B�fͬ�����ڏ��Ⱥ͕r���ϵąf�{�yһ��
NCPs�Y����D3��ʾ���ӑB��ɢ�䷨�y�����ļ{����Dp825 NPs��������7.17 �� 1.04 nm�����^ICP�������γɵ���K�ͺϼ{������������111.9 �� 37.10 nm������4.0������90���Ա�������������չ�F�����õķ�������Zeta�λ�����@ʾ��Dp825 NPs����늣�+23.6 mV�������γ�ICP���Ӻ��D������ԣ�-0.7 mV�������������L�w��ѭ�h���p�ٷ��خ�������������-��Ҋ�������V�@ʾNCPs��808 nm̎�����@������������900�C950 nm���γ��F�����շ壬���������D�Q�����������t����V�C����NCPs�и����ܽM�ֵijɹ��M�b��X�侀���估X�侀��������V�Y�����C�������ICP��λ�Y�����γ���

�D3. Dp825:ARS@PDA-Fe(III)-FA ICP NCPs���s����NCPs�����Ƃ��c������(A)Dp825 NPs��(B)NCPs������R�D��(C)NCPsԪ�طֲ��D��(D)�����ֲ���(E)90������׃����(F)Zeta�λ��(G)����-��Ҋ���չ��V��(H)�t����V��(I)X�侀�����V��(J)X�侀��������Vȫ�V��(K)��Ԫ�غ�(L)�FԪ�ظ߷ֱ����V��
�w�⌍�Y����D4��ʾ��������NCPs��PMN�ί����[�������딵���Ɲ�Ȟ�10.90 ��g/mL�������Ćδι���ί��r�g��10��犡���݆������-������ί��Y���pˎ���������Ɍ��������Խ���4.35%�������M�ֻ��ί��h��ȱʧ����������Ч��Calcein/PI�ɹ�Ⱦɫ���Y��Ҳ�C����ԓ�ί����Կ����w�⌍�F����ȫ���[������������e���ڸ߹��ʼ����Hһ݆�ί����o������[�������������Y��Ҳ�������������������@���۷eЧ����ԓ�ͺ��ί��wϵ���ИO���ąfͬЧ������ָ��CI=0.072�����h���چ�һ�ί��ֶΣ����w���[�������c�A���Ͱl�ṩ�ˈԌ����A��

�D4. Dp825:ARS@PDA-Fe(III)-FA ICP NCPs���s����NCPs���w�⯟Ч��(A)��ͬ�˚���NCPs̎�����[�����������ʺ�(B)��ȔM��������(C)��ͬ�˚���NCPs��PMN̎�����[�����������ʺ�(D)��ȔM��������(E)����ί��r�g������(F)�[������������׃��������(G)Calcein/PI�D��(H)�p�ɹⶨ���yӋ��(I)����ɹⶨ���yӋ��
�w�Ȍ��Y����D5��ʾ������С���ģ�����Y���@ʾ����ˎ��DOX��ARS�����һ̎�������ա����ˎ����y���@�������[�����[���w�e���L����ʼ�w�e�İ˱�����NCPs��PMN�Ϊ�ʹ�Ät�����L�����ڳ�ʼ�w�e���ı��ԃȡ��fͬ����Ч���@��������������NCPs + PMN�M��21��������F�����[����~300 mm3����100%�������[����������������TIR���yӋ�Mһ����C��ԓڅ�ݣ���ˎ�MTIR�H2.5%�C34.8%����W�R�M��29.6%��NCPs�M��PMN̎���MTIR�_68.4%��70.3%��NCPs + PMN�M��100%������չʾ���ͺϼ{������PMNϵ�y�Ϊ����õ��ί����ݣ���ͻ��չʾ���҂�����fͬ�ί����Եă�Խ�ԡ�60�����m�^������MIX + PMN��NCPs + OL�M�քe��62.5%�c50%�ďͰl�ʣ���NCPs + PMN�M�o�Ͱl���M���W�����@ʾԓ�M�[�������Y�������Ɖģ�δҊ��Ҫ���ٓp����ԓ���ԃHʹ��5.0 mg/kgˎ������鳣Ҏ��ˎ������1/10~1/20���h����������܄�����550 mg/kg����21���ί��ڃȸ��M�w�؟o���@�½�����ְl�]������ί����������W�ί��������ąfͬ�ί����ݡ��߸�Ч�Ͷ����������Ɍ��F�̈́�������Ч�ܵĂ��Ի����[���ί������R���D���ṩ������֧�Ρ�

�D5. �w�ȿ��[����Ч��(A)�[���w�e���L������(B)С���w��׃����(C)�[���|���yӋ��(D)�x�w�[������Ƭ��(E)60���[���Ͱl�yӋ��(F)��W�R�M�cPMN�M�[���ί�Ч�����ȣ�(G)�[���M����ƬȾɫ�D��
���P��������Molecular stacking@infinite coordination polymer nanocomposites for tumor continuous high-intensity photothermal-thermodynamic alternate cycle therapy and chemotherapy�����}���ڿ�ACS Nano���ھ��l�����ǵ�������������ΨһͨӍ��������ʿ���w���������µ�һ���ߣ�������ͨ��W�����t�W��Ϣ���̽��������c����Һ������WԺ��ԓՓ�ĵĵ�һ��ͨӍ���߆�λ��ԓ�о��ɹ��Džǵ��ν����n�}�M���[���fͬ�ί��I�����һ��Ҫ�Mչ��ԓ�����õ���������Ȼ�ƌW����81871476��32171388����������ʿ�����˲�֧��Ӌ����BX20220247�������ʡ���c�аlӋ����2022ZDLSF05-17���Լ����ʡ��Ȼ�ƌW���A�о�Ӌ����2022JQ-879�����Ŀ���Y����
ȫ��朽ӣ�https://doi.org/10.1021/acsnano.5c07772
- �Ϻ������fС�|���ڈF� Adv. Mater.�������-̼��λ�I�ľ��B���S��λ�ۺ��� 2025-03-28
- ���u��W������/���˂����� Mat. Sci. Eng. R�������w�S�^�������λ�ۺ���F�������Ĺ��fͬ���� 2024-09-07
- �K�ݴ�W�ɽ�ƽ���ڈF� JACS����λ�ۺ���ξ�ƽ�_�й�ظ߷��ӾۺϷ������y���߾���Ćξ��Y��������Ĺ��Cе�\�� 2024-09-04
- ����߿ƻ��W�WԺ�����۽����c������ JACS: �����͡��ø���{�ײ��� �� �I�������� 2025-07-20
- �칤����x/�R�w�R/���ƽ� Small����ˮ�˺�/�͜ع��fͬ�����[���ί� 2025-07-11
- ���ݴ�W�����ƽ��ڈFꠡ�Acta Biomater.����ˎ����;ۺ���{���z�������[���LЧ�ί����о��ɹ� 2025-07-08
- ����������W����÷���ڈF� AFM�����Խ�Ҝ����ޏ͡��ɻ����c�O�˜ض����W�����Եĸߏ��Ⱦ��受���w 2025-12-11
