������ί���PDT�����[���ί��о��ЏV���đ���ǰ����Ȼ�����ڷ��ӌ��������y���������[�������h�������@�������ί���Ч�����֮����I������������ه�^�ͣ����m�����m�ί������������й©�pʧ�������p���ί��ľ������c��ȫ���Ȇ��}�����⣬���Ҷ�����PEG������FDA���ʵ���������Բ��ϣ������ڼ{���d�w��������؏�ʹ�Õ��T����PEG���w�a�������l����ѪҺ�����ABC��Ч�����@��Ӱ푶�νoˎ�ί���Ч������ˣ���ο˷�������ه�ԡ����й©�Լ���νoˎ��ABC�F�����Ƅ�������ί����R�����þ�����Ҫ�ărֵ��
���գ��Ͼ��]늴�W�ܕ������ڡ��������I��W���IJ����ڡ�ɽ�|��W�������ں�������WJong Seung Kim�����о��F����_�l��һ�N����PEG�{���d�w�Ľ��t����^��NIR-II��������f��ϵ�y��KD1@HPEG NPs����ԓ�F��OӋ����������x������KD1����һ�����Ե���ӹ��wȡ�������l��܉���ؽM�����F������ه�Ĺ����Ч�����������й©�İl��������ZIF-8ģ�巨�Ƃ�İ���PEG�{���d�wؓ�dKD1������νoˎ�����ܱ��⿹PEG���w�Įa������Ч��Ҏ��ABC�F��İl�������F�؏ͽoˎ�µ��������ݣ��������[����λ����Ч�e�ۡ��о��l�F��KD1@HPEG NPs��ͨ�^�����w�����ϵK�cGPX4�{�ص��F�����pͨ·�fͬ�T���[��������������4T1���ٰ��б��F���������ί�Ч����ԓ�{���f��ϵ�y���������⻯�W�C�ơ�NIR-II���ӳ����c����ABC�F��Ķ��ع��ܣ����F�˿��؏��Ҿ��_���[���ί������Ƅӹ���������ṩһ�N��˼·��
2026��3��9�գ�ԓ��������Immune-Evasive NIR-II Nanoplatforms for Repeatable Photodynamic Therapy�����}�l����J. Am. Chem. Soc.�ϡ�Փ�ĵ�һ���ߞ�������W��ʿ������ɽ�|��W��ʿ��������ͳɶ���W������÷����

�D1. KD1@HPEG �{���w���ķ����OӋ�����ÙC�ƣ�ͨ�^�F�����C�ƌ��F���؏͵Ĺ�����ί���
�о��F��OӋ�ϳ��˹���KD1��ͨ�^���넂�Թ����ȡ����4-��������ȩ�����F�@����܉���ؘ���ԓ�����@�����M��I��ROS���ɣ��Գ�����x�Ӟ������ξ��B�����o����������Ч���Ʒ�ݗ��˥�p������Ƚ����й©�������D�QЧ�ʃH34.2%���h����ͬ�����������˷��خ��ԽM���p�����D2��������ZIF-8ģ�巨�����Ԍ�KD1��Ч�����M����PEG�{���w���У������������õĹ��Ч�����D3����
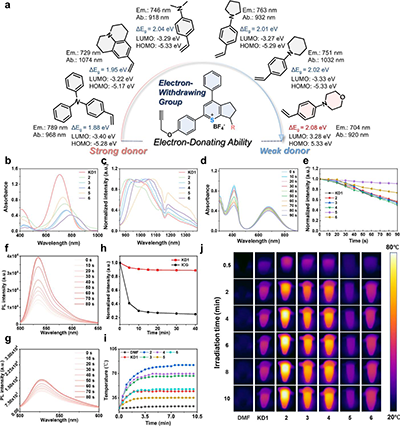
�D2. ���N��������x��������ģ�a�����ӽY������b������-��Ҋ���չ��V�Լ���c��808 nm�����µİl����V����d��ͨ�^DPBF��Ѫ�u��KD1�Ĺ�������ԡ���e���˜ʻ�DPBF ˥�p��������f��DHR123�z�yO2?�C�����ɡ���g��SOCG �z�y1O2���ɡ���h�����t��II�^��KD1�Ĺⷀ���ԡ���i��808 nm�����µģ�i�����ӟ������ͣ�i���D��
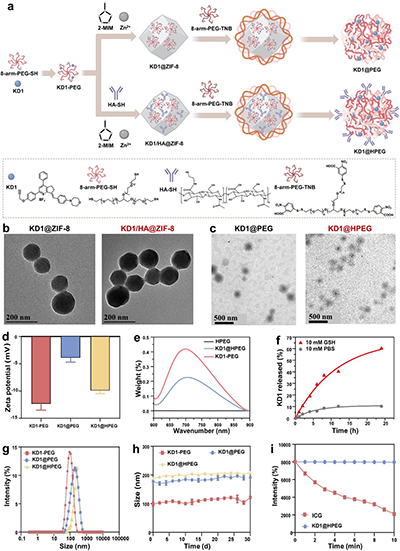
�D3. ��a������ZIF-8ģ���Ƃ�KD1@PEG��KD1@HPEG�{���w����ʾ��D��KD1@PEG��KD1@HPEG �{���w���ģ�b��ZIF-8 �D��ͣ�c��ȥ��ZIF-8���TEM�D��d��KD1-PEG��KD1@PEG��KD1@HPEG�{���w����Zeta�λ�ͣ�e������-��Ҋ���չ��V����f��10 mM GSH��KD1��ጷ��������{���w����g����PBS�е������ֲ������ͣ�h����PBS��30��ȵijߴ�ֲ�����i����880 nm����������KD1@HPEG��ICG �ğɹⷀ���Ա��^��
�w�⌍��C����KD1@HPEG NPs���[�������zȡ���ڼ��������¿ɴ�������I�� ROS��ͨ�^�����w�����ϵK�cGPX4�{�ص��F�����pͨ·�T���[������������ROS�Ɖľ����wĤ�λ���l�����w������ͬ�r���ļ�����GSH�����{GPX4���_������֬�|�^���������۷e����K���F�[�������ĸ�Ч�������D4����

�D4. ��a�������Ȼ��������ɵĈD��b��e��JC-1Ⱦɫ�D�����wĤ�λ�Ķ�����������c��f��C11-BODIPY�z�y֬�|�^������LPO����ˮƽ����d���c��a�����P�Ļ��������ȵĶ�����������g��i�������|ӡ�E�͟ɹⶨ���@ʾGPX4 �����{����h��KD1@HPEG+����M̎������TEM�D��j�����������z�y�Y����
ԓ�{���f��ϵ�y���ڶ��ע����܉����a����PEG���w��IgM��IgG��ˮƽ���@���������������[����λ�������õ�NIR-II����Ч�����C���������ABCЧ��������������؏�����ί��ṩ�������������D5����
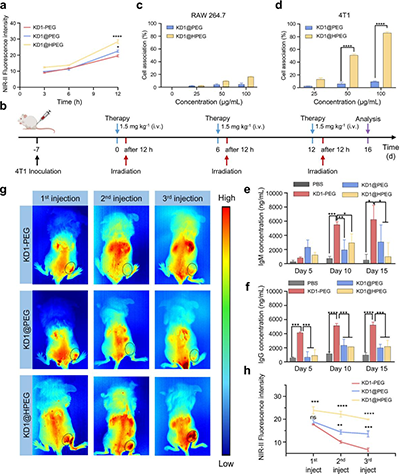
�D5. ��a���{���w��ע���3��6 ��12 h�����С���NIR-II�������yӋ����b����νoˎ���ί���������c��RAW264.7�ͣ�d��4T1������KD1@PEG��KD1@HPEG�{���w���Ĕzȡ����ע��KD1@PEG��KD1@HPEG�{���w����С���w�ȣ�e��IgM�ͣ�f��IgGˮƽ����g�����ע����С���w�ȵģ�g��NIR-II�ɹ⏊�ȈD��ͣ�h�������yӋ��
�����о������õ�������Ȼ�ƌW������Y����֧�֡�
ԭ��朽ӣ�https://pubs.acs.org/doi/10.1021/jacs.5c21383
- ��ɽ��W����ƽ/������/������ AFM��ͨ�^�{��늻��W�w�ƌ����پ�·��Ŀɿ����[���D����һ�N�Ԅ��|�l�����؏͵Ľ��پ�·�ޏͲ��� 2025-12-31
- �͵���W�������F� Angew���߾��ȡ����؏�ʹ�õ��܄��z�y������ 2025-08-25
- �A�ƴ�Ǻ��� Sci. Adv.�����؏�ʹ���������ϵ�y�����t�������O�y 2025-06-26
- ������Ĵ�W�����ڣ��Ʊ���Ժʿ�F� ACS Nano������AIEgen�Ŀ�Ҋ���������ӽM����Ⱦ�Ĺ�����ί� 2024-10-21
- �����Ӣ�����ڡ����ֽ��ڡ�Nano Lett.�������������N�����r�ЙC�Ǽܲ�������������������²��� ���Ŵ������ί�Ч�� 2024-10-21
- ������/�����/Ҧ�غ��� AM��DNA�{�ͺ������ڻ���ϵ�y������ί�ԇ���ɿع��f�� 2024-01-19
