����ʧ�����ɻ��ۺϣ�RDRP�����g������ԭ���D�����ɻ��ۺϣ�ATRP���Ϳ���ӳ�-������D�ƣ�RAFT���ۺϣ��ǘ������пɿط���������ֲ������W�M���Լ���ؓ��c�Y���ľ��_�ۺ���ď������ֶ��������@Щ���g�܉_�{�ض�N���w�wϵ���ۺ��^��������яV�������ڽ��湤�̡�3D��ӡ���ۺ���W�j����������ӡ�E�Լ��ۺ���-�������ż���I���ɻ���錧��RDRP�ژ������̻����Բ��Ϸ��������Ҫ�rֵ������䌢���\�g�c�߷������W��Y�ϣ����ڜغ͗l�����Ƃ�Y�����_�ľۺ���e�����ɻ��ۺ��^�̃��������������ԣ�RDRP�ڻ������еđ����ܵ��ˏV���Pע�����磬ͨ�^������RDRP�ϳɵľۺ�������ڼ������������湤�̣��������Ⱥϳɵľۺ���������{�������w�Ĺ����c�О飬�������������m���c�ɾ��������������s��ϵ�y����Բ��ϣ����ڼ����ί����t�W�I�����ڴ������wϵ��������ԭλ�l���ľۺϷ�����Ҫ���ⲿ�̼�����⣩�|�l�����������x���ۺ��^�̎����a��Ӱ푻��{�ء���ˣ�������������x;��ֱ���|�l���ڼ���ԭλ�M�е�RDRP�wϵ�����ںϳɾ����������������ܵĺϳɲ��Ͼ�����Ҫ���x��
Alexander��Keitz��Rawson���о��F�������������Ľ���߀ԭ���Ԍ��F����N����|�l��ATRP�^����Ȼ��������RAFT�ۺ���Ҫ���m�ṩ���ɻ��Ԇ��Ӳ��S�־ۺϣ��@���lչ����|�l��RAFT�wϵ��������������Qiao�n�}�M����������|�l��RAFT�ۺϣ���������ĩ����ӂ��f�߀ԭ��Դ�����ص��}���l�����Ķ����ɷ������ɻ��Ԇ���RAFT�ۺϡ��M�ܻ���܉�߀ԭ��Դ���ɻ����l���������ɵ����ɻ������¾ۺ������ӽY�����Ķ˻����|�Ժ��ۺ�朽Kֹ���Ķ�Ӱ��˸߷��ӵ��������W���|���������������߷��Ӳ����I��đ��á��e���ھۺϷ����^���У���Դ���l���a�������ɻ����H�������µ��ۺ�朣����l����Դ��朣�������Ŀ�˾ۺ���ķ�������߀�����½Kֹ朵����۷e����߾ۺ����ɢ�ȡ��@�N��������Ӱ���Ƕ�ι�������Ƃ����Ȟ����@����K�y�ԫ@��������Ƕ�ξۺ�����⣬�錍�F�^���ۺ��D���ʣ�RAFTͨ����Ҫʹ�øߝ�����ɻ����l�����@��������@�ļ������ԣ��Ķ����ƻ���|�lRAFT�ۺ��wϵ�İlչ��
��������Դ���l�����ۺ�������Ӱ푣�������lչ�˶�N��ه�ⲿ�̼�����⡢늣���RAFT�ۺ��{�ط������܉�ͨ�^�|�l����D��߀ԭ��D��ԇ����chain transfer agent, CTA���������ɻ����Ķ����lRAFT�ۺ�����ˣ�ͨ�^����߀ԭCTA�a�����l���ɻ������ɞ阋������|�lRAFT�ۺϵ�������ԡ�Ȼ����������l���£�����a����������w��߀ԭ�λͨ������CTA��߀ԭ�λ��������ڟ����W�ϣ�������w�y��߀ԭCTA�a�����ɻ����@Ҳ�ɞ阋�����ԭλ�|�lRAFT�ۺ��wϵ���P�I�y�}��
���ڣ��|����W�����ƌW�c�����WԺ/����W�ϳ����\�gȫ�����c��������ƈF�����늻�������ϣ���Ͼ���Shewanella oneidensis���İ���������f��extracellular electron transfer, EET�����|���_�l��һ�N�����|�l���ɿصĿ���ӳ�-������D�ƣ�RAFT���ۺ�ϵ�y���D 1����ԓ�wϵ�������̻�S. oneidensis ���ڵ��S������|���������S��riboflavin�����S�؆κ�����FMN��������ӽ��w����⼤�l�܉�ֱ�Ӹ�Ч߀ԭ���ɻ��ۺϵ�CTA���Ķ��a�����ɻ������Ӳ��S��RAFT�ۺϡ��Y������������ӂ��f���⼤�l�ąfͬ�C�ƣ�ԓ���g���Ա���ʹ�����ɻ��ۺϵ����l�����Ķ��������ϳɸ߷��ӽY���е��˻����|�������F�˸߾�����әC������Ч�{����ͨ�^�ϳ�����W�c�ۺϷ����Ľ����ںϣ�������һ��늻��Լ����ӵ����ɻ�RAFT�ۺ����ɳ��m���ɿص��ۺϷ���ƽ�_��
2025��11��21�գ�ԓ��������Photo-excited extracellular electron transfer of electroactive microorganism triggers RAFT polymerization�����}�l���ڡ�Nature Communications���ϣ�Nat. Commun. 2025, 16, 10257�������µ�һ���ߞ�|����W�����ƌW�c�����WԺ���ʿ�����_��W�����ƌW�WԺ��ʿ�����o��ʿ���κƽ��ڞ�Փ��ͨӍ���ߡ�ԓ�о��õ��ˇ������c�аlӋ���͇�����Ȼ�ƌW����ί��֧�֡�

�D1. ͨ�^���̸����Shewanella oneidensis �Ĺ⼤�l��������D�Ƙ���늻��������|�l�Ŀ���ӳ�-������D�ƣ�RAFT���ۺ��wϵ�����ȣ�ͨ�^�ϳ�����W����������Դ��Bacillus subtilis���S������flavins������ϳ�;���́�Դ��Pseudomonas aeruginosa�Ŀ���OprF��Դ���_��S. oneidensis���������S�صĺϳ��c������������Σ��S��������ӽ��w��������İ�������D�ƣ�EET���c���T������D�ƣ�PET����ϣ�����߀ԭ��D�Ƅ���CTA�������ʻ�������Ķ��a�����ɻ����|�l����錧��RAFT�ۺϡ���ԓ�^���У���ӂ��f;�������������E����i�����̻�S. oneidensisͨ�^D-������x�a������ӽ��^������ӂ��f�^�̣���ii���S�ؽ�EET�^�̱�߀ԭ����iii��CTA��PET�^�̱�߀ԭ�����w���ԣ�S. oneidensis���xD-�������a�����������ͨ�^�����|Ĥ����CymA���f���M��߀ԭ���|���ף��@Щ�����ٌ���ӂ��f��Mtrͨ·������ӽ�MtrA���f��MtrC��OmcA�����S������Mһ�����f��������Դ���ڵ��S�ط��ӡ�ͨ�^EET;�����S�أ�FL���M������߀ԭ��������ȫ߀ԭ�B���S�ؚ�����FLhq�����ڹ⼤�l�£�FLhq�γɹ⼤�l���g�wFLhq*��ԓ���g�wͨ�^PET߀ԭCTA���a�����ɻ�������RAFT�ۺϡ�
�ڂ��yRAFT�ۺ��У�������ɻ����l�����܌������a�����ԣ������¾ۺϮa��Ķ˻����|�ԡ���ˣ�������������Դ���ɻ����l������ه����������̽���������S�ؽ錧��늻��������������D���ӵ�RAFT�ۺ��wϵ���D 2a����Ȼ������ԓ�l���£��oՓʹ�ú��S��߀��FMN�����o�����F�ۺϷ������D 2b����ͨ�^ѭ�h��������CV���������S�ؼ�һϵ�� CTA ��늻��W���|��Ӌ��õ���FLhq��CTA������D�Ƶļ���˹��������GEET��������GEET > 0�����D 2c���������S��߀ԭ CTA �ķ����ڟ����W�ϲ����У������ԓ�l���o���������ɻ����l�ۺϡ����T������D�ƣ�PET����һ�N���V�����õęC�ƣ����܉F�����ڻ��B�o���M�е�����D�Ʒ�������˞�˷�����D�Ƶğ����W�ϵK����������FLhq�������������{�������£�ͨ�^PET�^��߀ԭCT�a�����ɻ����l�ۺϷ������D 2b�������Mһ���U�������C�������߲����ܶȷ�����Փ��DFT��Ӌ�����S�ؚ������l�B��FLhq*����߀ԭ�λ��Ӌ��õ��ļ��l�BFLhq*��CTA1��PET����˹��������GPET�քe�� -33.76 kcal mol?1��Riboflavinhq*���� -30.23 kcal mol?1��FMNhq*�����D 2c�����Mһ��֧����FLhq* ߀ԭCTA�ڟ����W���ǿ��еġ�
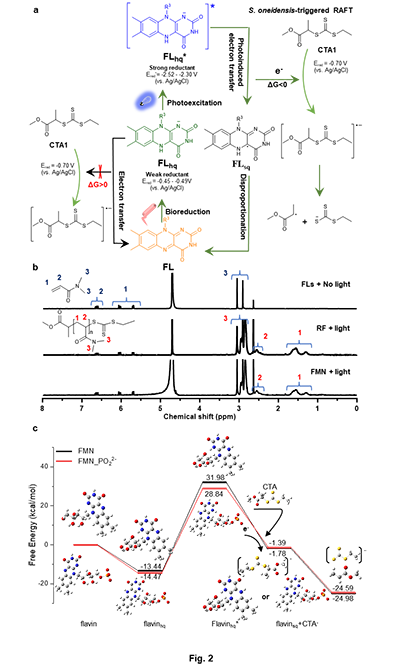
�D2. S. oneidensis �|�l��RAFT�ۺϵğ����W������
���˿�������錧�ľۺϷ����Ŀɿ��ԣ����߷քe�Ժ��S�غ�FMN������ӽ��w�M���˾ۺτ����W�о��������W�����������D3���������|�l�����ɻ��ۺϷ������Ͽɿ����ɻ��ۺϵ�����������ͨ�^���_�P���F�ۺϷ����Č��r�{�ء�ֵ��ע����ǣ��ھۺϷ����_ʼǰδ�^�쵽����PETRAFT�о��г�Ҋ���T���ڣ��Mһ���f��ԓ�wϵ�܉�����RAFT�ۺ��е����ɻ������^�̡��ڳɹ������S�ؽ錧��RAFT�ۺ��wϵ���Mһ���о�������S�؝�Ȍ�RAFT�ۺϵ�Ӱ푡���D3f��3g��ʾ�����S�؝�ȏ�0.2 ��M���ӵ�20 ��M�r���ۺϷ������ʳʾ������ӡ��M����RAFT�ۺ�����Դ�����̘I���ĺ��S�ػ�FMN�����@����߆��w�D���ʣ������鰺�F���ӄ��ijɱ����������ڴ�Ҏģ�ۺ��еđ��á���ˣ��_�lһ�N�܉�������Դ�S�غϳ������Ĺ��̻�S. oneidensis���꣬�����{��RAFT�ۺ��������P��Ҫ��
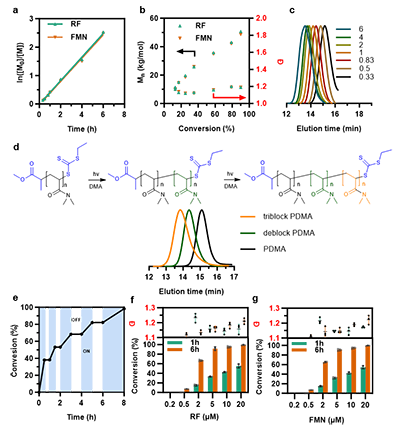
�D3. ����S�أ����S���cFMN���l����S. oneidensis�|�l��RAFT�ۺτ����W��
�������S. oneidensis�|�l��RAFT�ۺ��wϵ�е��S��ˮƽ�������_�l��һ�Nģ�K���ϳ�����W���ԣ��������S�ص�����ϳɺͿ�Ĥ�D�\���D 4�������Ȟ��������S������ϳ�;���ı��_�������S�خa����ϵ�y�о��������cS. oneidensis���ݵĆ����ӡ��Y�x�����̾���Ptet���S�خa���������ľۺ����ʾ��@����ߡ�Ȼ����OprF�����ؽMPtet���꣬�������S���D�\�����˱�������^�ȱ��_����ļ������ԣ��OӋ�����ɺ����w�Y��λ�c��RBS���{��OprF �ı��_ˮƽ���Y��������ͨ�^����OprF���_�����̾���P-RBS�ɼ����S�ش�Ĥ�D�\����߰����S�؝�ȣ��Ķ������ۺφ��w�D���ʡ��Mһ���u��P-RBS4�錧�ľۺτ����W���^�쵽���w�D�����S�����r�g�ʾ������ӣ��������ֲ��S�D����׃��Ҏ�ɷ��Ͽɿؾۺ����������о�EET�M�֣���c-Cyts����RAFT�ۺϵ�Ӱ푣��҂��Mһ���������ó��ض�c-Cyts���ۺτ����W��Ӱ푡��Y������c-Cyts�ڌ���ӏļ���ݔ���������S���е��P�I���ã�����ͨ�^�z�������M����Ч�{�ء�

�D4. ��S. oneidensis�M�л��̸����Ԍ��F�������S�ص����^�ϳ��c���ڣ��Լ��䌦RAFT�ۺφ��w�D���ʵ�Ӱ푡�
�C�����������ߘ�����һ�N��늻�������S. oneidensis�|�l��RAFT�ۺ��wϵ��ԓ�wϵ�܉�ͨ�^����ֱ��߀ԭCTA�����Y�Ϲ����l�B�m�a�����ɻ����Ķ�����ۺ����ж˻����|�������S��RAFT�ۺϵ��M�С���������߀ԭ�c�⼤�l�fͬ���ã�ʹ����܉�ļ�����Ч�D����CTA���˷��˼��������S��ֱ��߀ԭCTA�����R�ğ����W�ϵK������ԓ���̻���S. oneidensis�ӾۺϷ����wϵ�����߳ɹ����F�˶�N���w��CTA��RAFT�ۺϣ��@���ˆη�ɢ�����õľ������Ƕ�ι��������w�D���ʿɸ��_ 99%����ɢϵ����D���ɵ���1.11���@һ�����|�l��RAFT�ۺ��wϵ���ɞ錍�F��������錧RAFT�ۺϵ������ֶΣ���������չ��������w�����wϵ��
ԭ��朽ӣ�https://www.nature.com/articles/s41467-025-65119-x
- �|�ϴ�W�����۽���/������� Small���t��⼤�l�ğoˎ�ﴩ���z���ί����o�}Ѫ˨���о� 2024-03-23
- ���ϴ�W�����á������˹��WФ�� CEJ���⼤�l��ͺϽ�{���غ��/�����/ˎ�����ϯ������M��Ⱦ��Ƥ�w�M���ޏ� 2024-02-08
- ��ɽ��W�����������n�}�M AM���չ⼤�l��С�r�����L���x�ۺ��ﱡĤ 2024-02-03
- �|�A��Wë��������ٻ AFM���{���i����늻��Է��� - 늴ŸБ����M���������Ϻ͂����h���O�y 2025-08-08
- �|���ִ����½��ڈFꠡ�Adv. Sci.�����w�S��/ľ�|�ػ�ꖘO�ď�����׃�֏��ϻ��Ļ�����B늻�������Ĥ 2025-05-15
- �������������/����/�w�� AFM�����нM���ܷ�ʹ���Ѫ���ԵľW�j���ܡ�늻��ԺͿ���������z - ����ֹѪ�ʹ��MƤ�w�������� 2025-04-08
- �����̄���|��ʩ��/�͵���W�ױ� Angew���ۺ���댧�w�{���R�_���F��ͨ���ɿ����S�\���c������ 2025-08-27
