�������ܓp��������h������ͨ�^늴̼����ޏͣ������y���ص��Դ��K���R�����á����⣬���ߌ�����Σ�U��B�ĸ��X�ϵK�Ͳ���Ҋ�����˂����o�����y�Ⱥͽ���ؓ�������ˑ����@Щ�������о��_�l��һ�N����늴ŸБ�Ч������늵�늻��Է��ϣ��Ɍ��F�o��늴̼��ί��͂����h���O�y��ԓ�о�ͨ�^�o늼��z���g���o늇��F���g�ąfͬ���ɣ�����Ti3C2Tx MXene��PCL�w�S֮�g�γɵļ{�����i�Y���x�������σ����ęCе���ܺͷ����Č���ԣ���3.5 S·cm?1��PBS��Һ����7������ʞ�72.2%����������늴ŸБ�Ч���a����10.8 ��A�ğo��������ɹ������˶�N��������̖ͨ·��calcium��TGF-����PI3K-AKT��PPAR��Axon guidance��Wnt����ͬ�r�����װY���P����̖ͨ·��TNF��NF-��B�����c���սM��ȣ��@�N�����О�������h�����p���{���քe���M���������Ϻ���������36.3%��283.8%����߀���ԱO�y���ڜضȡ���׃���B��Һ��������̖�����F���r�;��_�Ă����o������֮���@��о����M��늴ŸБ������t�W�͂��Ի��t���İlչ��

�D1 늻��Է��ϻ���늴ŸБ����M�����������ϼ��h���O�y
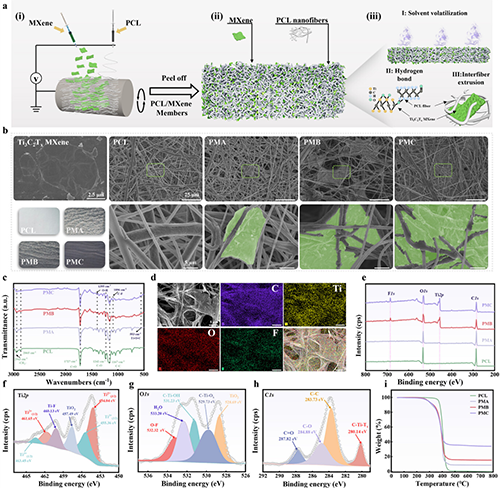
�D2 늻����w�SĤ���Ƃ��c����

�D3 늻����w�SĤ�ęCе�����͟o������yԇ

�D4 늻����w�SĤ���w���\��O�y����

�D5 늻����w�SĤ����늴ŸБ��a���ğo�����̖�������О����{��
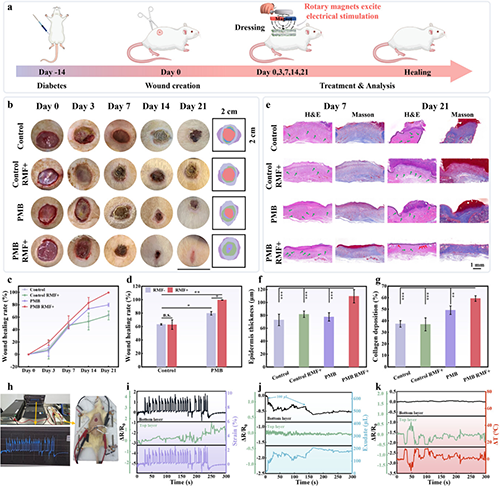
�D6 ����늴ŸБ��T���ğo��������M����������������

�D7 �������ϵ����ߟɹ�����

�D8 ���ڽM��RNA���Йz�y����
�����ɹ��_�l��һ�N����늴ŸБ��ğo�����Թ�늡�늻��Է������������������������������Ϻ�����Ƥ�w�ؽ������܉�O�y�����h��׃����Ti3C2Tx MXene�cPCL�w�S֮�g�γɵļ{���i�Y��ʹ���Ͼ��Ѓ����ęCе���ܺ͌���ԡ��w��/���о�������늻����w�SĤ����늴ŸБ�ԭ���a���ğo�������Ч�{���������О飨��ֳ���w�ƺͷֻ�����RNA�y��Y���C����N��̖ͨ·���}��TGF-����PI3K-AKT��PPAR��Wnt�������������{TNF��NF-kappa B�� IL-17 ��̖ͨ·���@�������P����ı��_�l��׃���ͼ������ӵ�ጷţ��Ķ��p�p�װY���������M��������|���ܡ��������ϡ���ë�ҵ�Ƥ�w����������������⣬����늻����w�SĤ���ضȡ���׃�͝B��Һ�����푑��ԣ��ɹ����F�ˌ������h��������̖�ıO�y���������t������߂����o�������ľ��_�Ժ�Ч�ʷ�����M���������ش�ؕ�I��ԓ���ԓ��б�y���o�����o���ă��ݣ������бO�y�������@���������߂��������еľ��Ý�����
Փ�ĵ�һ�����ǖ|�A��W��ʿ���ܷ�P����ͬͨӍ���ߞ�|�A��Wë�����о��T����ٻ���о��T��
Փ����Ϣ:
F. Zhou, L. Wei, L. Tang, M. Shan, Z. Wang, J. Peng, Z. Zhang, X. Liu, Q. Zhang, F. Wang, L. Wang, J. Mao, Nano-Interlocking Enhanced Electroactive Dressing: Electromagnetic Induction for Accelerated Diabetic Wound Healing and Wound Microenvironment Monitoring. Adv. Funct. Mater. 2025, e08829.
ԭ��朽�:https://doi.org/10.1002/adfm.202508829
- ���T��W�ܱ����n�}�M ��Nano Energy��������늴ŸБ�����푑���ָ���ӷ���������˙C�������� 2022-08-10
- ���ݴ�W���Ӱ��о��T�F� AFM��һ�N�������������Ե���λ���u���V�V�������r�ЙC���ˮ���z���ڴ��M���������� 2025-05-06
- �|�ϴ�W�����۽���/������� CEJ�������NƬ�c늴̼��fͬ�{�������h�� ���M��Ⱦ���������� 2025-02-17
- �����츣��/���Fꠡ�����tԺ���� Biomaterials��ؓ�dС�މA�z��������푑���ˮ���z���M���������� 2025-01-02
