���T��W����·�n�}�M Adv. Mater.�����ͽ���-��ӾW�j����STINGͨ·�����[�������ί�
2022-01-04 ��Դ���߷��ӿƼ�
����������߯������d���׃�˰��Y�ί���ģʽ��Ȼ�����[���������������h�������ܰͼ�����������ʹ�[��׃���䡱���������߯�����푑��ʲ����ߡ�������о��������ɔ_�ػ���̼����ӣ�stimulator of interferon genes��STING��ͨ·�ļ����܆��ӿ��[����Ȼ���ߑ���ʹ���䡱�[���D���顰�ᡱ�[�����Ķ�����[�����ߌ����߯�����푑��ʡ����y�ķ����ί����T�����|dsDNA���γɣ��M������STINGͨ·������֮�⣬�Ϊ����i�x��Ҳ������STINGͨ·�ļ������ӡ��b�ڴˣ����T��W����·�F�ͨ�^ʹ�û��W�ϳɵ�����������c��N�����x����λ������һ�N���ͽ���-��ӾW�jDSPM������STINGͨ·�����[�������ί���

�Dһ. ����-��Ӽ{�W�j�Ę����Լ�����W����
ԓ�о��И����ă��H��PEG-����ۺ������c�|ϵ�{��������λ�����F����ˮ���|ϵ�{�������D׃���Hˮ�ļ{�����ӣ���ʣ��ķ��u���Mһ���c�i�x����λ�γ�DSPM����-��ӾW�j���[�����������ԭh����ʹԓ����-��ӾW�j���w���Ķ�ጷų�DSNPs���i�x�ӡ���X-ray�����£�DSNPs����ů��������T�����������������γɼ����|dsDNA���c��ͬ�r��ጷŵ����|���i�x�Ӽ���cGAS���ҘO���������䌦���|dsDNA��푑�����������STINGͨ·�����M��ͻ����ij��죬�Mһ�����[���خ��Կ�ԭ���f�oT���������������[�������_�������h���[����Ч����

�D��. ����-��Ӽ{�W�j�ı���
ԓ�о��Mһ���U���˝��ڵ��ί��C�ƣ��C�����[���h����STINGͨ·�ļ����Լ���ͻ����ij��졣С�����ٰ�ģ�͵������ί��Y���@ʾ��DSPM�Y��X-ray�����ܴ�ʹ�[����ļ�����T�ܰͼ�����ጷŴ����Ĵ��������ӣ������[���h����ʹ���䡱�[���ɹ��D���顰�ᡱ�[����
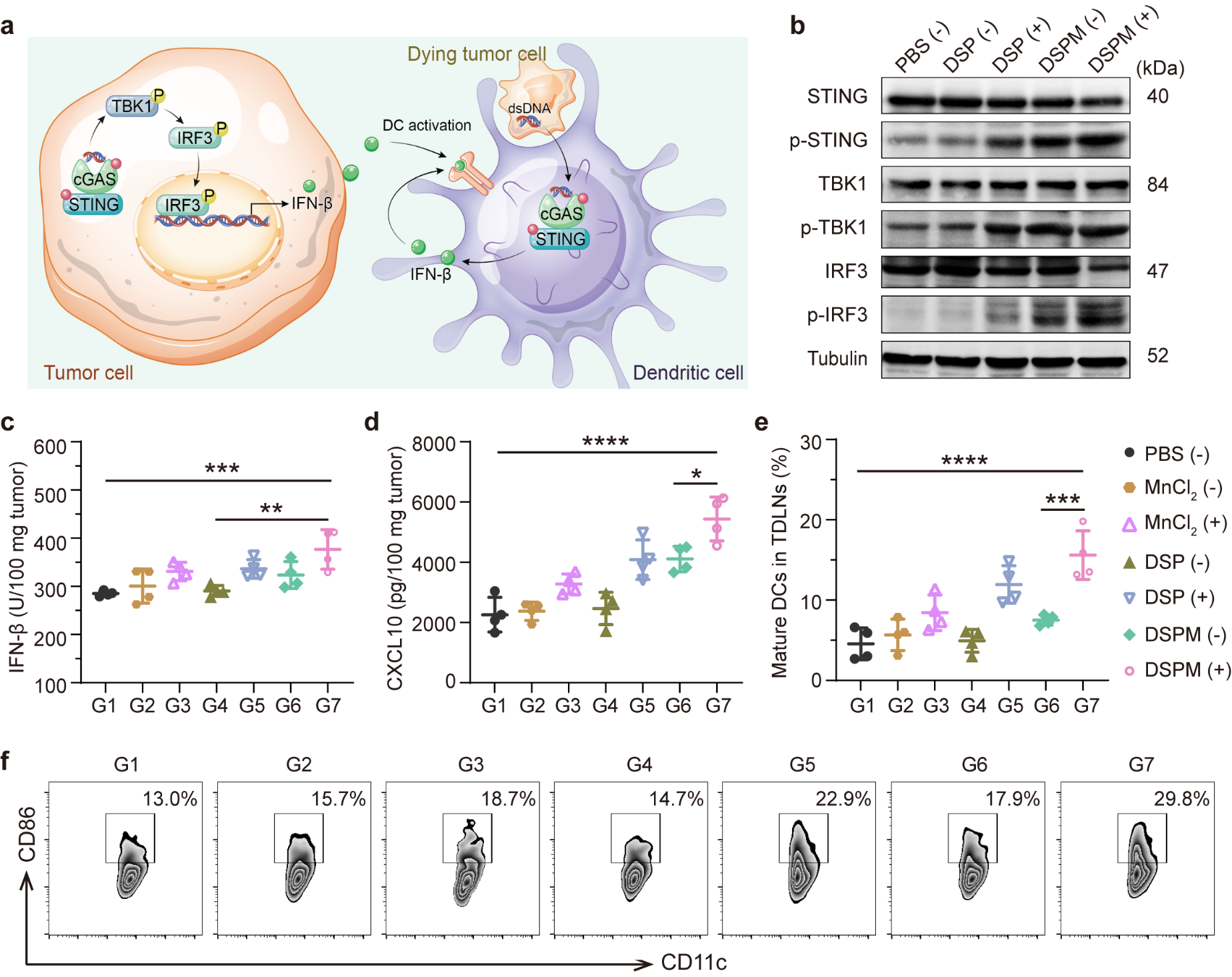
�D��. ����-��Ӽ{�W�j�����[���h��STINGͨ·��DC����

Փ����Ϣ Jie Yan, et al. Engineering radiosensitizer-based metal-phenolic networks potentiate STING pathway activation for advanced radiotherapy. Adv. Mater., 2022DOI: 10.1002/adma.202105783
ԭ��朽�: https://doi.org/10.1002/adma.202105783
����c��؟�����Ї��ۺ���Wԭ�����¡������ý�w�����D�d��Ոϵ�]�䣺info@polymer.cn����Ոע����̎��
��؟�ξ���xu��
���P��
- ��������ǵ��ΈF� ACS Nano�����Ӷ���@�o����λ�ۺ���ͺϼ{�������F�[���B�m�ߏ��ȹ��-���������ѭ�h�ί��ͻ��� 2025-08-01
- ����߿ƻ��W�WԺ�����۽����c������ JACS: �����͡��ø���{�ײ��� �� �I�������� 2025-07-20
- �칤����x/�R�w�R/���ƽ� Small����ˮ�˺�/�͜ع��fͬ�����[���ί� 2025-07-11
- �|�A��Wʷ��ꖽ��� Nano Today����������-��ӾW�j�������Ե��טӶ����z�����Fԭλ�X�z�|��������/���W����/�����ί� 2025-05-28
- �|�ϴ�W�����۽����n�}�M Small���������ϽM�b����-��ӾW�jһ���Ƃ书���Գ����z�� 2023-08-30
- ���T��W����·�n�}�M Adv. Funct. Mater.������-��ӾW�j�{�ױÌ��F�[�����ؚ������� 2022-02-16
- ���������ѡ������T��W����·�F��аl�����ͷů�ˎ�� 2023-03-20
