���g�г����ί�ԭ�l�����ٰ��Ę˜��R�����ԣ����������ٰ��g��Ͱl���D�Ƶİl�����^�ߣ�Ŀǰ�R���ϳ���ȡ�g���o�������ķ�ʽ�������[���Ͱl�c�D�ơ�Ȼ�����ɻ���ˎ��a���ĸ����úͲ��l�Y�������»����g�������|���½������⣬�[���������е����u�ԕ������g�К�����[�����u�܇������M����ʹ�[�����ض����ٰl���h���D�ơ���ˣ������[���g��Ͱl�c�D�ƣ������o�������ĸ����ã�������g�������|����ؽ����Q�Ć��}��
ᘌ��@һ���}�����Ͻ�ͨ��W�ܽB�������F��_�l��һ�N��������ˎ������ֲ��ʽ�༉�Y���w�S�b���������ٰ��g���o���ί���ԓ�b���ж༉�Y���w�S�Ȳ������������Ų����ɲ�ͬ���������Ҷ�����PEG�����ɵ�ǻ�ң����ڰ��d�Hˮ��ˎ���}�ᰢù�أ�DOX·HCl�����w�S���w�ɾ����ᣨPLA�����ɣ����ڰ��d��ˮ�Ի��|���ٵ���ø2��MMP-2�����Ƅ��p�����DSF����ͨ�^�{���γɃȲ�ǻ�ҵ�PEG����������ʹDOX·HCl����ጷţ����ڃȚ����g��δ�ص��г��Ě����[������ֹ�[���g��Ͱl��DSF�t���S�w�SPLA���|��������mጷţ��LЧ�����[���������ڵ�MMP-2���ԣ���ֹ�[�����܇������M�����u�������[���h���D�ơ�
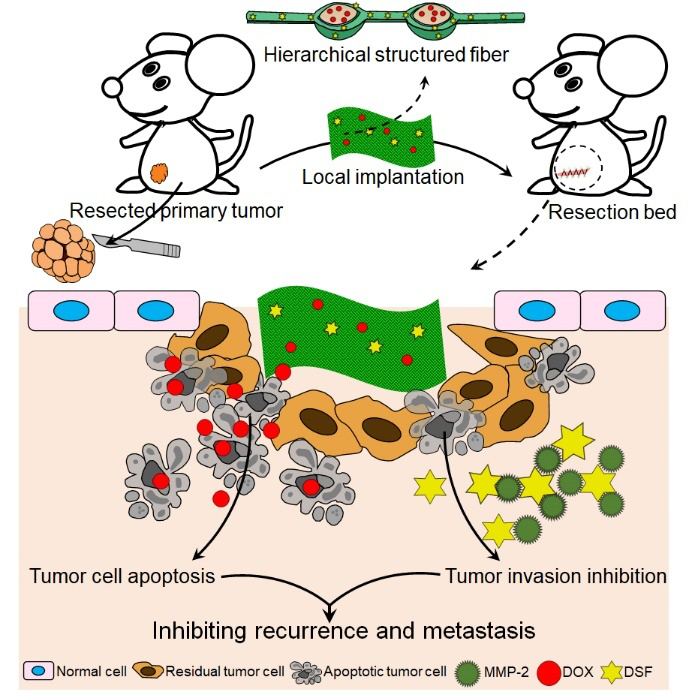
�D1 �Ȳ�����ǻ�ҵĶ༉�Y���w�S�b�õ��Ƃ估�������[���Ͱl���D�Ƶ�ʾ��D��

�D2 �༉�Y���w�S����ò������PEG���������w�S��ò��Ӱ푡�
�w�Ȍ��Y��������ԓ�b��ͨ�^�ھֲ�����f���pˎ������ԭ�l���[���g��Ͱl���D�Ƶ��L�U����Ч��������g�ί����g���o���������ί�Ч���������w�S�b���ί��ĺ���С������60.0%����ȫ�������Ͱl�[���������_90.3%���ί�С��42��r����ʞ�100%�������zԭ���ߟɹ�Ⱦɫ�����ԽM����С��β���H&EȾɫ��Ƭ������ԓ�w�S�b�õ�����ˎ�О���Ч���������[�����ڵ�MMP-2���ԣ���ֹ���[������������������|�е��zԭ�ɷ֣��Ķ��������[�������u���D�ơ��ҽ����w�S�b���ί���С����ڃ�δ���Fˎ��a���ļ��Զ��ԣ��L���ί���Ҳδ���F�����@��ȫ�����ԡ�

�D3 �༉�Y���w�S�b���w�������[���g��Ͱl�c�D��Ч���u�r��
���ϳɹ��l����Adv. Funct. Mater.(2020, 2004851)�ϡ�Փ�ĵĵ�һ���ߞ����Ͻ�ͨ��W���όWԺ��ʿ����������ͨӍ���ߞ��ܽB����������ͬͨӍ���ߞ����Ͻ�ͨ��W��ⲩʿ��
Փ��朽ӣ�https://onlinelibrary.wiley.com/doi/abs/10.1002/adfm.202004851
- ��ʿ�m��W�w��ϼ���ڈF�ANGEW������J-�ۼ��ğɹ�������D��(FRET)���g�O�y���dˎ�ۺ���{���w����ˎ��ጷ� 2020-08-13
- ���ϴ�WѦ�i�����ڡ����S܊���ڈF��������Q�z����֧�ܘ��������ģ�߷���ȡ�����Mչ 2019-02-28
- ��������ǵ��ΈF� ACS Nano�����Ӷ���@�o����λ�ۺ���ͺϼ{�������F�[���B�m�ߏ��ȹ��-���������ѭ�h�ί��ͻ��� 2025-08-01
- ����߿ƻ��W�WԺ�����۽����c������ JACS: �����͡��ø���{�ײ��� �� �I�������� 2025-07-20
- �칤����x/�R�w�R/���ƽ� Small����ˮ�˺�/�͜ع��fͬ�����[���ί� 2025-07-11
- �пƴ�������/���/�Y��F� Science��ϵ�y��ʾ�߷����d�w���ϰl��ϵ�y������ĵәC�� 2026-03-20
- �㽭��W�������ڡ�����ܽ��ڈF� JCIS�����ڰ�ȫ�Ź������ʹ̼�푑�ˎ���f�͵ļ{������ 2025-09-09
