���ڵĸ��|���ޏͲ��H��Ҫ�M�������]�ϣ�����Ҫ���װY�{�ء�Ѫ�������c���|���ܵȶ�������W�M���M������f�{��Ƥ�w��Ĥ�{����༉���{�ͺ��w�S�W�j�Y�������ޏ����ڿ����鼚���w��ͨ������̖���fý����R�r���|��Դ���Ķ����������ޏ��M�̡���ˣ��_�l�܉�ģ�M��Ĥ�Y�������F�r���Ը��A�ķ��������wϵ�������Ƅӂ������Ϗĺ��η��]�~��������������Ҫ���x��
���ڣ���ɽ��W�h���c���W���̌WԺ�����F�ͨ�^ģ�MƤ�w��Ĥ�ӵĶ༉���w�S�W�j�Y�����Ƃ�����ں˚��{���w�S�ďͺ�ˮ���z���ϣ�CA-DAF-BSA@PFD�����錍�F���Ԃ��ڵĸ��|�������ṩ����˼·���D1����
2026��1��15�գ�ԓ�����ԡ�Bioinspired Hydrogel Prepared by Core-Shell Nanofibers: Accelerating Wound Healing via Macrophage Polarization Modulation�����}�l���ڡ�Advanced Functional Materials���ϡ�

�D1����Ĥ�����{���w�Sˮ���zʾ��D
ԓ�о��Ծ������������������c������Եļ���ϩ��������ܛ���أ�CA������ˮ���z���|��ͬ�rͨ�^ͬ�S�o늼��z���g�Ƃ����Լ���ϩ�����Ͼ��Ǟ隤�ӡ����d������ͪ���{���w����BSA@PFD����˵ļ{���w�S�W�j��������R�c����R�����Y�����������ü{���w�S���������ĺ˚���ò����һ��ֱ���ߴ磬���dˎ�{���w�����w�Sо�ӃȲ��ֲ����D2������ˎ��Ŀɿ�ጷŵ춨�˽Y�����A��
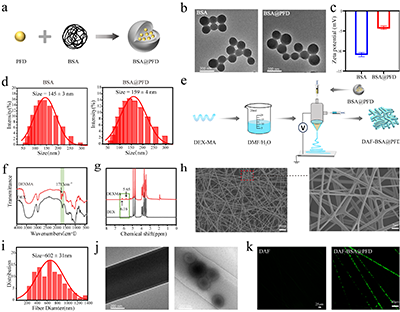
�D2���dˎ�{���w�S���Ƃ����
�龫��ģ�M��Ĥ�M�����{�༉�Y�����о��Mһ���������dˎ�{���w�S�cCAˮ���zǰ�Һ�ͺϣ���ͨ�^�⽻�γ����S�ͺ�֧�ܡ�ͨ�^�����{���w�S�z��ˮ���z�еı������ͺϲ������^��ò����ӽ���Ȼ��Ĥ���w�S?���z�ͺ����������ں��^�ϼ�����õĿ�ע���ԡ��m�˵����W���ȡ������Ŀ���Û�������D3�����Ķ�������ޏ��ṩ����������W�h����
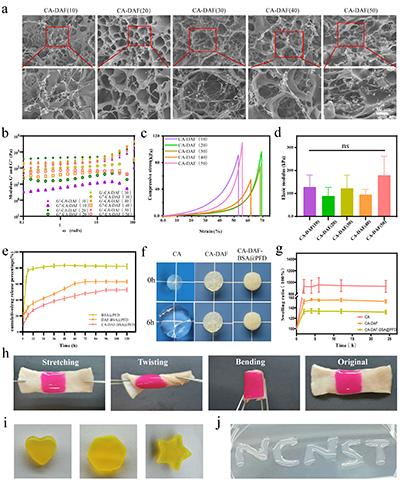
�D3���{�ͺ�ˮ���z���Ƃ����
�w�⼚������@ʾ��ԓˮ���z�܉���Ч�������ɼ������ס����ޏ͵�M2���͘O����ͬ�r���Ƴ��w�S�������^�Ȼ�ļ����w�S�����ֻ�������ԓ���Ͼ߂�f�{�װY�����c���Ʈ����w�S�����p���{���������ڴ���ȫ��Ƥ�wȱ�pģ���У�ԓˮ���zչ�F���@���Ĵ�����Ч����һ����ͨ�^���MѪ�ܻ���ѿ�M�������c��Ƥ�������ل����]�ϣ���һ����ͨ�^�r��ጷ�ˎ����Ч�����zԭ���^�ȳ��e�c�����Ɂy���Ķ��@���p�p���γɣ��D4����
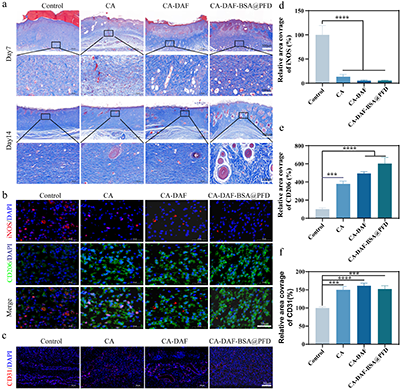
�D4��ˮ���z�������h�����{��
�C��������ԓ�о�����ͨ�^����ķ����OӋ����ģ�MƤ�w��Ĥ�Ķ༉�w�S�W�j�Y�������ںϿ�ע��ˮ���z�c�dˎ�˚��{���w�S�ă��ݣ��ɹ��_�l��һ�N�߂�r���Թ����{�������ďͺ�ˮ���z��ԓ���ϲ��H�鼚���ṩ�����������֧���h�����������Ӹ��A�����M�̣�ͬ�����M�M�������c�������γɣ��錍�F�����y���ς��ڵĸ��|���ޏ��ṩ��һ�l������Ҫ�D��ǰ�����²���;����
ԭ��朽ӣ�https://doi.org/10.1002/adfm.202524234
- �A������߅�������w�i������������ڈF� Nat. Chem.���_�l����ˮ�¡��f���z�� - �`��Դ�Ժ������� 2026-03-31
- ���t��һ��Ժʢ�������/�A�ƴ��R������ AFM�������˷������ˮ���z�NƬ-�ڼ���p���ί�����ȡ�����Mչ 2026-03-02
- ����������·���ڈF� AFM���ġ����顱���ֵ��IС������{���w�SĤ - ���F�{��Һ��ͨ�����x 2026-02-25
- �����w�n�}�M Macromolecules����/�Ņfͬ�{��-�˚��Y��Fe3O4@��ܗ�ۺ�����p�T��ATRP��øż���� 2025-04-25
- ����̫/�����F� Sci. Bull.�������pЧ���������ȼ�Եĺ˚��Y��BN/SiO2�{���w�S̫����sĤ 2025-01-10
- ��۳��д�W����ɏ���ڈFꠡ�ACS Nano��: �}⁵V�{���T���ĺ˚��o�C�ЙC�{���w�S���ڸ�Ч�����ռ����Թ�늱O�y 2024-03-26
- �K�ݴ�W�̽z���ڈF� Small�����Џ���/����M�ϽY���ĸ�Ч���}�{���w�Sˮ���z��̫������l�� 2025-05-06
