Ƥ�wȫ��ȱ�p���[�������ĵ����ֿ��Ǻ�ɫ�����g��Ͱl�������T����Ȼ����Ŀǰ���g���o������ͨ��ᘌ���һ���أ������˻��߂��w����£��[�������������ޏͺ������{��֮�g�ď��s������������ȱ�����g���h���ӑB��׃�ĕr���{�أ��@ʹ���y���Ƅ�������ѭ�h������ѭ�h���IJ������D�����¾��ʸ��A�ɞ��y�}���eʧ����ί�����
�b���������}��������W����淽��ڡ��ݿ�������ͻ������ڈF������ϡ�������ø���ԵĽ��p��ˮ���z��ͨ�^������ɫ�����g���ί��]�h�����D���퐺��ѭ�h���Ą������ԡ�
ԓ����ͨ�^�ЙCģ�巨���|ϵԪ���B�����s���~��������Բ����У��S���������L�����������ӣ�APAP�����ٌ��@�õ��w�����b��ϯ��A�I���W���Ľ��p�Ͱ��������z��Gela-Amino����ˮ���z֧���С�ԓˮ���z���p���C�ƣ����ڃ�Դ���ԭh��/��Դ���t�⣨NIR���̼��r���|�l�[����������/�F����/�~�������������ģʽ��ͬ���錧�����h�������c���M�M���ޏͣ���Ч�ƽ��g����s���������������y�ĺ�������
2026��1��8�գ�ԓ��������Disentangled Hydrogel with Rare Earth-Activated Multi-Enzymatic Activity Reverses the Pathological Vicious Cycle by Establishing a Closed-Loop for Postoperative Melanoma Treatment�����}�l������?Advanced Functional Materials?���ϡ����µ�һ������������W�����WԺҦ���Ჩʿ��ԓ�о��õ�������Ȼ�ƌW����ί��֧�֡�
�����c
ԓ�о���ˮ���z��M3%Cu/3%Eu@A GOC���Ľ��p�ض��M�о����{�أ����ض��i�����p�ȹ��������ί������s45�������˜ض��£�M3%Cu/3%Eu@A GOC��NIR�������l�����p�О飬���Fˮ���z���S�ΑB���ؘ����������ܺ������ӽM����ͬ�r���FM3%Cu/3%Eu@A���[���Ͱl�ں͂��ڸ�Ⱦ�A�ε�����/���ӔUɢ�������OӋ��M3%Cu/3%Eu@A��NIR�̼��£�����������������ܼ����f��Ч�����@��������ø���ԣ��_���˹������a���u�����ɻ���·OH�������Ĺ����ģ�GSH���ļ�����朡����У��o��ǰˎAPAP���[���ă�Դ���Ұ���ø�c�wϵ���o��O2���D��鶾�������x�ͬ�r�ӄ�GSH�Ľߺ�ROS�U�����T�����Ŵ��~����/�F����/���fͬ�Ļ�ϼ�������ģʽ���@����������ˎ�Ժ�ɫ�����Ě������á��������A�Σ�M3%Cu/3%Eu@A GOC�Kֹ��������ģʽ���{�����ɼ������ͣ�ጷ����ڱ�Ƥ�ؽ��Ĺ����Խ����x�ӡ��@һ���¼����ʴ��[���г����ȫ���̣������˃�Դ����̖�c��Դ��NIR�fͬ�{�ص��ί�������ѭ�h��
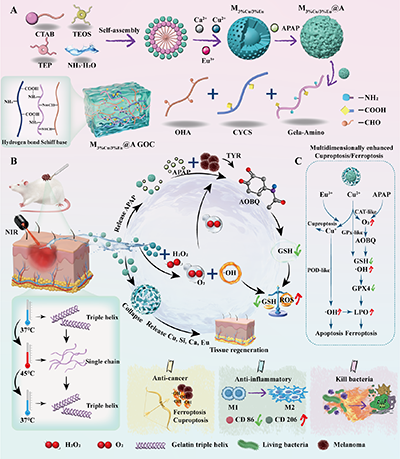
�D. ��S����������/���ӽ����{�ͺ�ˮ���zϵ�y���F���Ժ�ɫ�����g���ί��ĝ��ڙC��ʾ��D��
�D�Ľ��x
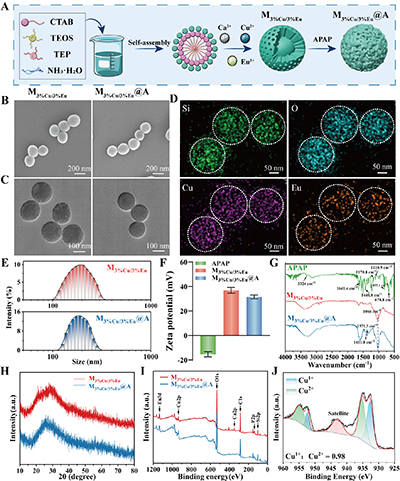
�D1. M3%Cu/3%Eu@A���Ƃ�ͻ��A������A��M3%Cu/3%Eu@A�ĺϳ��^��ʾ��D����B���ͣ�C��M3%Cu/3%Eu��M3%Cu/3%Eu@A��SEM��TEM�D��D��M3%Cu/3%Eu@A��Ԫ��ӳ��D��E���ͣ�F��M3%Cu/3%Eu��M3%Cu/3%Eu@A�������ֲ��D��Zeta�λ����G��M3%Cu/3%Eu��M3%Cu/3%Eu@A��FTIR����H��M3%Cu/3%Eu��M3%Cu/3%Eu@A��XRD�D�V����I��M3%Cu/3%Eu��M3%Cu/3%Eu@A��XPSȫ�V����J��M3%Cu/3%Eu@A��Cu2p�ľ����V�D��
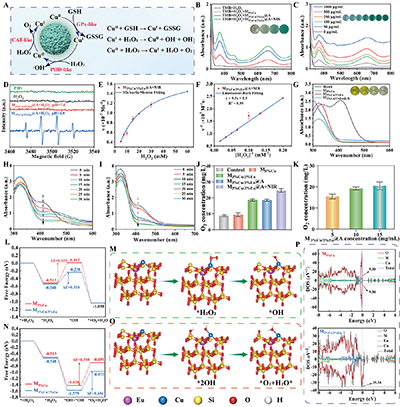
�D2.��A��M3%Cu/3%Eu@A��ø�Ӽ�ʾ��D����B��M3%Cu/3%Eu@A��^������ø��POD�����ԡ���C��M3%Cu/3%Eu@A ��Ȍ�?OH����Ч�ʵ�Ӱ푡���D����ͬpH�l����M3%Cu/3%Eu@A�������������ESR�����V�D����E��?OH��ʼ���������cH2O2��ȵ����τ����W������������������F��Lineweaver�CBurk�p�����D����G���{���w����GPx���ԡ���H��M3%Cu/3%Eu��GPx�����S�r�g��׃����������I��M3%Cu/3%Eu@A��GPx�����S�r�g��׃����������J��M3%Cu/3%Eu@A��O2����������K��M3%Cu/3%Eu@A�ĝ����ه��O2����������L��M5%Cu�cM3%Cu/3%Eu��CAT���Դ��^�������܈D����M��M3%Cu/3%Eu��CAT���Է������Eʾ��D����N��M5%Cu�cM3%Cu/3%Eu��POD���Դ��^�������܈D����O��M3%Cu/3%Eu��POD���Է������Eʾ��D����P��M5%Cu�cM3%Cu/3%Eu�đB�ܶȣ�DOS���D��
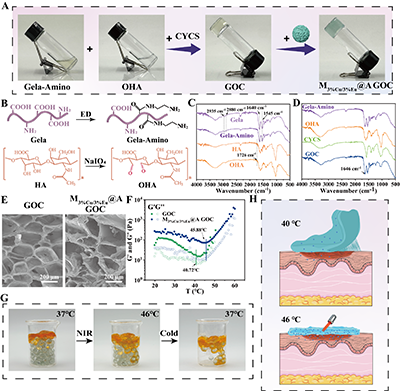
�D3. ˮ���z���Ƃ�ͱ�����A��M3%Cu/3%Eu@A GOC�ĺϳ��^��ʾ��D����B��Gela-Amino��OHA�ĺϳ�ʾ��D����C����ͬԭ�ϵ�FTIR���V����D����ͬԭ�Ϻ�ˮ���z��FTIR���V����E��GOC��M3%Cu/3%Eu@A GOCˮ���z��SEM�D����F����25��50��֮�g��GOC��M3%Cu/3%Eu@A GOC����׃�ضȒ��衣��G��M3%Cu/3%Eu@A GOCˮ���z��NIR�ӵ��ΑB�D׃����H������M3%Cu/3%Eu@A GOCˮ���z�ܜضȿ��ƽ��p��ʾ��D��

�D4 ��A����ͬ̎��l����B16F10������[Ru(dpp)3]Cl2Ⱦɫ�Y���ͣ�B��������ԅ^��Ķ��������Y������C����ͬ̎��l����B16F10������DCFH?DAȾɫ�Y���ͣ�D��������ԅ^��Ķ��������Y������E����ͬ̎��l����B16F10������C11?BODIPYȾɫ�Y���ͣ�F��������ԅ^��Ķ��������Y������G����ͬ̎��l����B16F10�����ľ����wĤ�λ׃����r�ͣ�H��������ԅ^��Ķ��������Y������I�����սM�cM3%Cu/3%Eu@A GOC+NIR�M�g����_����DEGs����ɽ�D����J�����������c����M�ٿ�ȫ����KEGG�����������D����K�����սM�cM3%Cu/3%Eu@A GOC+NIR�M�g����_����DEGs���Ļ�����������GSEA���Y������L���P�I����_����DEGs����D��

�D5 ��A���ί�����ʾ��D����B���w�ȹ���ί��ğ����D����C������ί���Ĝض�׃����������D�����M��������w�|��׃����������E����14�섃�x�[���M���Č���D����F�����M��14����[���|���yӋ�Y������G��CD8?T�����cCD4?T��������ʽ�����g�����Y������H��CD8?T�����г������������w1��PD-1�����_ˮƽ����ʽ�����g�����Y������I��CD80?CD86?�p��Լ���ռ�ȡ���J��CD8?T�����Ķ��������Y������K��CD4?T�����Ķ��������Y������L��PD-1���_ˮƽ�Ķ��������Y������M��CD80?CD86?�����Ķ��������Y����
����Y
���о�������һ�N��S�����Ͷ�ø����ˮ���z�wϵ��M3%Cu/3%Eu@A GOC�����о��C�����ڽ��t��⣨NIR�������£����о�������ˮ���z���l�����p�c����׃�������H�Ɍ��F����Ӳ�Ҏ�t���ڵĶ����m������䣬߀���ڏͰl/��Ⱦ�A�Ό��Fˎ�������/���ӔUɢ���ھ����OӋ��M3%Cu/3%Eu@A�{���wϵ�У�߀ԭ�Խ����x�ӳʬF�����صăr�B�D׃�����t�������ɴ��Mԓ�{���wϵ��������ܼ��D����Ч���İl�����M���������ø���ԣ������^������ø��POD�����������^������ø��GPx�����^������ø��CAT����ģ�M���ԡ����⣬�o��ǰˎ�����������ӣ�APAP����ͨ�^�[����Դ���Ұ���ø��Tyr���c�wϵ���o�����⣨O?���ąfͬ���ã������D����ж�������x��Ķ���ֹ��Դ�Թ����ģ�GSH�����~�������������á��@һ�^�̕��ӄ������ĵ������c��������ROS���ĔU����ͨ�^�~�������F�����c���Ч���ąfͬ���ã���Ч�T�����Ŵ�������
��K��������Ч���a���˶�ģ�B�����Ӵε��ί�Ч�������ʽ�Q�˺�ɫ�����г��g���M���еĸ�����𡣳���APAP�⣬�����ğo��ǰˎ���T����Ҳ��������δ���c�{�ײ��ϵ�ø�Wҕ���õĺ��x���Ԍ��F���V�����[���]�h���������ţ����о��_�l���wϵ���H�ǹ���{�ײ��Ϲ�����չ�ĵ���������Ҳ�������ˎ���[���ͽM���ޏ��I���ṩ���P�I���b��
����朽ӣ�https://doi.org/10.1002/adfm.202531433
