�����|ճ�τ�ͨ�^���汩¶����ˮ���cճ�ϻ��F�錧��������ã����������ڟo��ĵ����|�Y���S�����۾W�j���Ķ�չ�F�����ŵĝ�Bճ������Ȼ�����ڳ�Ҏ�����|�wϵ�ЏͬF�@Щ���������R�����������ڽ���̎������ˮ�����������W�j�Ⱦ������档���о����һ�Nͨ�ò��ԣ��_�l������չ�_�����|��ճ�τ������þ��������L机�늺��ܶȵľ�늽��|���F���i��������늽��|�cչ�_�����|֮�g�@���������o��c���I����ã�ʹ����ܷ���չ�_�����|��¶����ˮ����������ͨ�^��p�Y�����W�j�Ⱦ������@�N��늽��|-�i���ķ��ӹ��̲��Ԟ��OӋ���Ѓ�����ճ�����ܵĵ����|��ճ�τ��ṩ��ͨ�ÿ�ܡ�
2025��12��22�գ�ԓ�о��ɹ��ԡ�A Universal Polyelectrolyte-Locking Strategy: From Common Proteins to Stable Unfolded Protein-Based Adhesives for Rapid and Robust Tissue Sealing�����}�l����Advanced Materials��Adv. Mater.��DOI��10.1002/adma.202511921�����㽭��Wë�������ں�����ɯ�о��T��Փ�ĵ�ͨӍ���ߡ�
�����ͨ�����|ͬ�r������ˮ������ճ�����ܻ��F����O��/��늰����ᣩ��������Ȼ�ۯB��B�£���ˮ����ʼ�KǶ��o���������Y���У�����Ķ����Y���t������朵������ԡ���ǰ�о����������W׃�Ԅ���������2-���һ���좡������Ҵ������أ���ͨ�^�����|չ�_���r��¶��ˮ���ճ�����F��Ȼ�����@ЩС������ˮ�Е����ٔUɢ���M�����l�����|��ˮ̮���;ۼ�����K�ƉĽ�����ˮ�ԾS�֙C�ƣ��D1A��B������ˣ���ͨ�����|Ҫģ�M�����|ճ�τ����R�ɴ��P�I����1��������¶��ˮ�����Ԍ��F�־õ��Ž���Һ�w���ã�2��չ�_�����|��Ч��p�Y�Ԍ��F������ɢ��
�ڱ��о��У�ë���������n�}�M�_�l��һ�Nͨ�õľ�늽��|-�i�����ԣ����ø�늺������Եľ�늽��|�i��չ�_�����|���r��¶����ˮ������߀ԭ��Ȼ�����|�еĶ����I���a�������Bչ�_����ʹ��ˮ������ճ���Թ��܈F��¶�ڱ��棨�D1A������늽��|���������g����ã����o����á����I��������չ�_��B�����F�p�����i��������i���S�ֱ�����ˮ�ԣ���ii�����Fչ�_�������Ч�p�Y���D1C������������ճ�τ��܌��F���ٿ�����Һ�w�ܷ⣺������ˮ���Fͨ�^������ˮ���Ž���ѪҺ���wҺ��ʹճ�ϻ��F�c�M�������γɷ���ճ��������늽��|�i����չ�_������p�Y�t�����˃Ⱦ����ܣ��D1D����

�D1. ������չ�_����ճ�τ��OӋ��
���о������x����ţѪ����ף�BSA���;۱�ϩ�ᣨPAA���քe����ģ�͵����|�;�늽��|���������ԽM��ճ�τ���UBSA-PAA�������ӄ����Wģ�M�Y�������C���ˣ���늽��|ͨ�^�o����á����I�����Լ�����ˮ̮���������ƣ������ˁ����Bչ�_�����|��ˮ�����ı�¶���Ķ����늽��|-�i����չ�_�����|ճ�τ������˙C�ƻ��A���D2����

�D2. ͨ�^���ӄ����W��MD��ģ�M����������չ�_����ճ�τ���
���������о��OӋ���Ƃ���������չ�_����ճ�τ�UBSA-PAA���D3����չ�_�����|��UBSA����PAA�g�����@�������ĽY���H��������Y���H����������ԭʼ�����|��BSA����PAA֮�g���߳����ɂ���������1.05×108 M-1 vs. 1.51×106 M-1�������ڴ��������ķ���չ�_����ճ�τ����F��Խ�ı�����ˮ�ԣ�ˮ���|��>90�����c�Ⱦۏ��ȡ��������UBSA-PAAճ�τ������r�������٣��������K��Ƣ�K���κ��I�K�����F�����ŵ�ճ���������ڝ��iƤ�ϵĴ�Ӽ��У����Џ��ȣ�63.07 �� 6.52 kPa����T�̈́��xճ���������g�ԣ�86.07 �� 24.68 J m?2��������ճ���yԇ�����쏊�ȣ�104.50 �� 3.65 kPa)���о�չ�F��������ճ�����ܣ����̘I�w�S�����z��3�����ϣ��D4�������ϽY������f���˾�늽��|-�i�����Եă��ݡ�

�D3. ������չ�_����ճ�τ����OӋ�c�Ƃ䡣
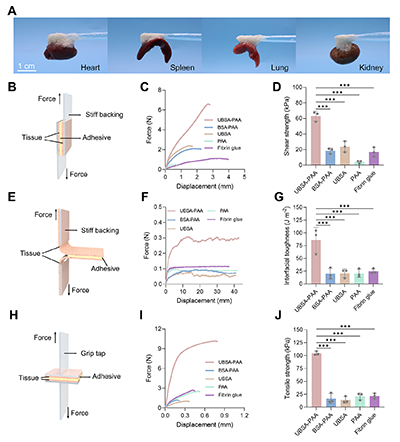
�D4. ճ������
���⣬���о�ϵ�y�Ե��u����UBSA-PAA�wϵ֮��Ķ�N�����|-��늽��|�M������C����늽��|-�i�����Ե����m�ԡ�����չ�_����ճ�τ���չ�F�����ڌ���ԭʼ�����|-��늽��|�M�ı�����ˮ�ԡ��Ⱦۏ��ȼ�ճ�����ܣ��D5����

�D5. ��늽��|-�i���OӋ���Ե����m��
ͨ�^����Ƥ��ֲ��ģ���о���UBSA-PAAճ�τ��w�����オ���Ժ��������������D6����UBSA-PAAֲ����ʬF�u�M���|���pʧ��ֲ��8�ܺ����ȫ���⡣�M���W�u���@ʾ�p���װY�������c�����w�S�����z�^�쵽�Į��ﷴ�����ơ�CD68�cCD�Ķ������ߟɹ�����@ʾ��UBSA-PAA�M�c�w�S�����z�M�ı��_ˮƽ�ஔ���@Щ�C���u���C����UBSA-PAAճ�τ���߿ɽ��������c���������ԣ��M���R��ճ�τ����õĺ��Ę˜ʡ�ֹѪ����ͨ�^�ڃɷN���K��Ѫģ�ͣ�ʧѪ���p��92�C95%��ֹѪ�r�g��10�����D7����һ�N���عɄ��}��Ѫģ�ͣ�ʧѪ���p��88%��ֹѪ�r�g��50�룩�еõ���C���c�����w�S�����z��ȣ�UBSA-PAA���F����ѪҺ�_ˢ���������ι̵��ܷ�������

�D6. �����������c���オ����

�D7. ������K��Ѫģ�͵��w��ֹѪ���
���о������ڽ�Q�����|��ճ�τ��OӋ�е�һ���P�I������ͨ�^��늽��|�i��չ�_�����|�Է����䕺�r��¶����ˮ������ͬ�r�������ϵ����w�Ⱦ����ܡ������о��m���õ����|׃�ԕ��r��¶��ˮ�^������ȱ����Ч�ķ����C�ƣ����ڝ�B�h���еđ����ܵ����ơ���늽��|-�i������ͨ�^��չ�_�����c��늽��|�fͬ�Y�Ͽ˷����@һ���ޡ�����֮�g�������o�������c���I���F���p�ع��ܣ����������̎������ˮ��������ͨ�^��p�Y�����Ⱦ�����ԓ���������m��Դ��������OӋԭ�t����i����늽��|朵����Լ�늺��ܶ��cչ�_���ĽY��������ƥ�䣻��ii��������ˮ���c���w�Ⱦ����܅fͬ�Y�ϣ��Ķ����ֿܵ�����Һ�w�ɔ_�����ܷ�ֹ���ϱ��wʧЧ�����о�ͨ�^�C�����m�ľ�늽��|�Ɍ������Bչ�_�����|�D���鹦����������ϣ����OӋ���ճ�τ�������һ�����ƏV��ͨ�ÿ�ܡ�
ԓ�о��õ��ˇ�����Ȼ�ƌW�����㽭ʡ���c�аlӋ�����㽭ʡ����ָ���ط��Ƽ��lչ����Y����Y����
Փ��朽ӣ�https://advanced.onlinelibrary.wiley.com/doi/10.1002/adma.202511921
- �������/̫ԭ�������P���F� Macromolecules���}���s��늽��|ˮ���z�ڟ�̼��µķ�ƽ��푑��О� 2025-12-11
- �A��������W�ב����� Macromolecules��ͨ�^������늽��|늺������{���p늌���������� 2025-07-21
- �A���삥/�����ֿƴ����H� AM���p�ظ������������i�������������S����������ľ�R�� ֮��-�����{���c����Ⱥ�������˝����ԽY�c�� 2025-06-09
- ���ݴ�W�Ε���/������ Adv. Mater.�������ӏͺ�ˮ���z�i����x������\�x��늳�ѭ�h���� 2025-04-21
- ����/���ƴ�����F� Small: Һ�������w�з����_�P�������О�ĄӑB�����i�� 2025-03-14
- ����������é�|��/ꐺ����F� Mater. Horiz.: ���i���������x�ӏ����w 2024-10-31
- �����ֿƴ��䏩/�ǫI�¡�����������ꐝ�/Ф�i��Nat. Commun.��: �nj��Q�H��ˮ���|�Y���ӿ���ˮ�Uɢ - �s��ˮ���z���F��Ч���ˮ�ռ� 2026-04-02
