��ϼ�����Ⱦ�������Ǹ��m����Ծ���G+���c���m����Ծ���G-����ͬ���l�ĸ�Ⱦ���DŽ����o���I���һ������������Ҫԭ�������y��һ�����د����y��ͬ�r��������l�]���������������������ڽoˎ�������s���y���ڕr������Ч�fͬ����ˎ�Ȇ��}��ᘌ��������}������������W���d���ڈF��_�l��һ�NpH푑��͟o�d�w�{��ˎ�PBN����ԓˎ��ͨ�^�ӑBϯ��A�I�ϲ��ԣ�����ճ����B��PMB�����G-���c��ȩ�����������X����BF�����G+���ԽM�b�ɼ{���w�����Դˌ��F����ϸ�Ⱦ�ĸ�Ч�ί����D1�����о��@ʾPBN�ܽ����o�����������ڼ������棬�Ķ���߾ֲ��ί����ĝ�ȣ��ڸ�Ⱦ��λ�������h���|�l�£�PBN��ͨ�^ϯ��A�I�Ĕ����خ���ጷ�PMB��BF���քe����������ˎ�~�G�نΰ�����MDR-PA��G-����������ˎ���Sɫ���������MDR-SA��G+�����cPMB/BF���pˎ�Ͻoˎ��ȣ��{���ԽM�b�γɵļ{�Y����PBN�ڌ���������ϸ�Ⱦ�r���F�����ߵį�Ч��ͬ�r߀�@�������˿����������ϼ�����Ч�����ɹ����F�ˌ�С���ϼ�����Ⱦ���ڵ���Ч�ί����ڻ�ϼ�����Ⱦ�ί����@ʾ�����õđ��Ý�����

�D1.PBN�����ϼ�����MDR-SA/PA�����M�������ϵ�ʾ��D��
����Ҫ�c��
��1��PBN�fͬ��Ч���MDR-SA/PA��ϼ�����PBN��MDR(SA/PA)����С�־���ȼs4��g/mL��������PMB/BF������4����������С������ȽY���@ʾPBN�ڝ�Ȟ�10��g/mL�r��������л�ϼ������@��PMB/BF�Ě���Ч�������2�������⣬���L�����Y���@ʾ���ڝ�Ƚ�����8��4��g/mL�r��ֻ��PBN�������@���Ŀ���Ч������PMB/BFδ�����ƶ�����ˎ����SA/PA�������L������PBN���^�͝�����ܸ���Ч������G+/G-������������L���D2����

�D2.PBN����ϼ�����������ˎ���Sɫ��������Ͷ�����ˎ�~�G�نΰ����������Ч����
��2��PBN��Ч�Ɖ�G+��G-�����ںͼ���Ĥ�� PBN̎���@�������MDR-SA��MDR-PA��Ĥ�λ�����¼���Ĥȥ�O����ͬ�r���F�ˇ��صı�Ĥ���s���ܓp������й©�Y���@ʾ��PBN�M�ĵ����|й©���@�����ڌ��սM������PBN̎�팧�¼����ںͼ���Ĥ�ć����Ɖġ����������|��й©���ӣ���K���¼����������D3����
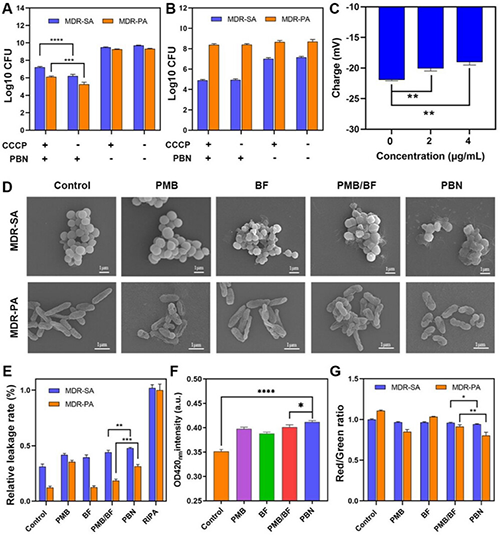
�D3.PBN�����MDR-SA��MDR-PA�ęC���о���
��3��PBN��������w�Ȼ����Ⱦ�����M��������������С��Ƥ�w���ڻ�ϸ�Ⱦ��MDR-SA/PA��ģ�ͣ��ί��о��@ʾ��ˎ̎����PMB/BF���̎�팦���ڻ�ϼ�����������÷dz����ޣ���102 CFU������PBN�M���F����͵ļ������������Ă����]���ٶȣ���102 CFU���Լ��ڻ֏��ڼ��ٵ��w�����L�����@���������M���D4����

�D4.PBN���w�Ȃ��ڻ�ϼ�����Ⱦ���ί�Ч���u�r��
�C��������ԓ�о������һ�N��������������ϸ�Ⱦ�����ق������ϵ����͟o�d�w�{������PBN���cPMB/BF���pˎ�Ͻoˎ��ȣ�PBN�������ԽM�b�ļ{�Y�����ڌ���������ϸ�Ⱦ������F�����ߵį�Ч����K���ق������ϡ�
���⣬ᘌ�G+��G-�����Ⱦ���o�d�w������ͬ��ʩ���p�����ص���⣬�ڱ�����Ч�Ե�ͬ�r�����ɷֵ�ȫ���ã����ˎ���������öȣ��p��ˎ�����ͬ�r�������ί���Ч�����p����Ч��������ˣ����о��鄓���o�����ί�������ϸ�Ⱦ�ṩ��һ�Nȫ�µĽoˎ�²��ԡ�
���P�о��ɹ�����DualAntibiotics-BasedpH-ResponsiveCarrier-FreeNanodrugagainstBacterialMixedInfectionforAcceleratedWoundHealing�������}�l���ڌW�g�ڿ�AdvancedHealthcareMaterials������Փ�ĵ�һ���ߞ鱱��������W�����ƌW�c���g�WԺ�о������������������ͨӍ���ߞ�����������W���d���ڡ�����h�����ں��x���������ڡ�ԓ�о��õ�������Ȼ�ƌW������Ŀ���Y���c֧�֡�
�n�}�M�Wվ��http://www.wangxing-lab.com/team.aspx?pid=2510
����朽ӣ�https://doi.org/10.1002/adhm.202501845
