��ᯟ����PTT���Ǽ{���t�W�I���ǰ�ؼ��g��ͨ�^���_�ļ������䣬�a���ֲ��ߜ����簩������Ŀǰ���������ů������g�г��ǂ��y�İ��Y�ί���ʽ�������������ړp�����������Լ����l���Ի��t�lȫ�����ԵĆ��}�����^֮�£�PTT�����Ч�Ժ͌������M������С�����ԣ���ԭλ�ΰ����\����ί��ķ�����о�ĝ�����Ŀǰ��PTT���о���Ҫ�����ڽ��t��һ�^��NIR-I��700-1000 nm���������t�����^��NIR-II��1000-1700 nm�������ڜp�ٌ������M���Ĺ�p�������Ӵ�����Լ����������pʧ����ă��ݣ������ܵ���ҕ�����^�ڟo�C���ϣ��ЙC�������ڽY�������ԡ���ȫ�Ժ����������Է���ռ�Ѓ��ݡ����ǣ��ЙC���t�����ղ����N��^�٣��ҷ����Բ����_�l���н��t����^���������ⷀ���Ե����Ͼ�����Ҫ���x��

���գ�����������W��÷ؑ�����n�}�M�c���R��˼���ʿ˸߷����о���Klaus M��llen�����Լ�ϣ�D�s����{��WGeorge Floudas���ڈ����һ�N�������ý��t����^���յ��ЙC������V��TMI�����������QFTQ������ԭλ�ΰ��Ĺ���ί���ͨ�^��������ܗ�L�Ⱥ���������������ã�FTQ�����շ��_����1140 nm����������1500 nm�����⣬�����^���ķ��Ӄ�늺��D�ƣ�FTQ߀չ�F��14.4��0.4 Debye�ĸ�ż�O�ء����w����C����ͨ�^�cDSPE-PEG2000�ԽM�b��FTQ�{���w���@ʾ�����õĹⷀ���Ժ����������ԡ���1064 nm���������£�FTQչ�F��49%�ĸ߹���D�QЧ�ʡ��w����w�Ȍ���Mһ����C��FTQ�{���w����ɫ�����������ԡ�����ί���Ч��������������С��ԭλ�ΰ�ģ���У�����FTQ�{���w���Ľ��t����^����ί������ڹ�����������³ɹ���ʩ��

�D1. ����FTQ�{���w���Ľ��t����^����ί�ʾ��D���DƬ��Դ��J. Am. Chem. Soc. 10.1021/jacs.3c11314��
FTQ��������շ�λ��1140 nm(NIR-II�^)���������w������������ṩ�˿��ܡ�ͬ�r���F��14.4��0.4 Debye�ĸ�ż�O�ء�

�D2.��a��FTQ���Ӻϳ�·������b��TQ��FTQ�����չ��V����D:TQ����FTQ���ң�����c�������Y����ģ늹��V�y����ż�O�ء�
�cDSPE-PEG2000�M�b��ˮ���Լ{���w����FTQ NPs������1064 nm���������£�FTQ NPs�����^�ߵĹ���D�QЧ�ʣ�49%���������Ĺ�᷀���ԡ����⣬���w��PA����Ҳ�ܙz�yԭλ�ΰ��[�����@Щ�Y������FTQ NPs�ڐ����[���ί��о��Н��ڃrֵ��
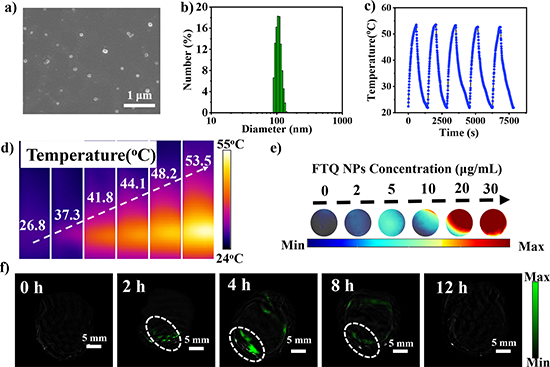
�D3. ��a�� FTQ NPs��SEM�D��b��FTQ NPs��DLS����c������ݗ��(1064 nm, 1.0 W cm-2) 5��ѭ�h��FTQ NPs�Ĺ�᷀���ԡ���d����������10 min��FTQ NP��Һ����ȏ����ҷքe��0��2��5��10��20��30 ug/mL���ğ����D����e����ͬ���FTQ NPs�w��PA�D��f��ԭλ���[���M���в�ͬ�r�gFTQ NPs���w��PA�D��
��1064 nm���������£�FTQ NPs��Hepa1-6��MCF-7��A549���������F�������ļ��������ԡ�����Annexin V-FITC�͵⻯����M�м�������/��������ʽ�����g��������������r��1064 nm���������FTQ NPs�T��2.5%�����ڵ���������16.5%�ĉ���������79.0%�����ڵ���/�������������֮�£�FTQ NPs��NIR-II����Ϊ����䶼�������Ƽ������L���@Щ�Y���C����FTQ NPs��Ч���w��PTT���á�
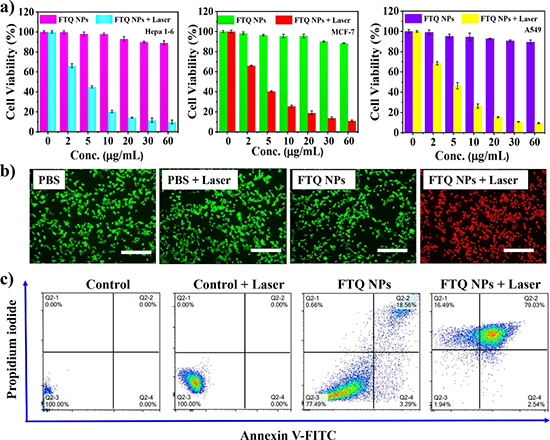
�D4. ��a��Hepa 1-6��MCF-7��A549�����ڲ�ͬ��ȵ�FTQ NPs�£���1064 nm���������µļ�������ʡ���b���}�G��-AM(�Gɫ)�͵⻯���(�tɫ)��Ⱦɫ����ͬ̎����Hepa1-6�����ğɹ�D�ȳ�: 125-um.��c��ʹ��Ĥ����VFITC�͵⻯��व���ʽ�����g������������/������
�����õ�PCE�������ԡ����������Ժ�PA���������Ĺ��裬��1064 nm����������FTQ NPs�M����PA��������PTT���w���о����c��ס�M��G1����ȣ����M��G3���Ĝض����@���ߵ�53.5 oC����T = 19.5 oC�����@����FTQ NPs���w�ȵĹ���D�Q����Ч�ģ����F����NIR-II������������Ч�������[����

�D5.��a����ͬ̎���MС���ڵ�0��4��8��12��16��20�������l��D��b��ԭλ�г��ĺ������K����c���ί�20�����K�Ĵ�����H&EȾɫ�D��d�����[�����L��������e���w��׃������f�����ί��MС������
ԭ��朽ӣ�https://pubs.acs.org/doi/10.1021/jacs.3c11314
ͨӍ���ߺ���

��÷ؑ������������W�����c�ƌW���̌WԺ���ڣ���ʿ�����������x���ҡ��f��Ӌ�����I܊�˲ţ������s�@��ʮ���á��Ї�����Ů�ƌW�Ҫ������ھŌá���°��Ƽ����ª���������������WУ�L������Ƹ����Ѫ�ܼ���2011�fͬ�������ġ�Ƹ�Ό��ң����x�Ƽ�����������Ƽ������I܊�˲š����������������o�����˲š����о������ɹ�-���{�ײ��ϵĘ����c����W�����о������ɹ�-�����F���ܸ߷����ЙC�Y�ϣ�������ϵ��ˮ���Ժ˚��ɹ��ؓ�{�ײ��ϣ����F���خ��ԟɹ���Ә�ӛ�����Ϳ���ˎ�P��Ό�[���ȡ��Ե�һ��ͨӍ������Nat. Commun., Chem. Soc. Rev., Acc. Chem. Res., J. Am. Chem. Soc., Angew. Chem. Int. Ed., Adv. Mater., Prog. Polym. Sci., ACS Nano, Chem. Sci., Small�ȌW�g�ڿ��ϰl����140��ƪSCIՓ�ġ�
- �п�Ժ�Ϻ��ЙC����ϣ���о��T�c�Ʊ���Ժʿ�F����ڴ�WAIE�о����� Angew��ͨ�^�{�����w�������������ܽ��t����^�����ЙC�댧�w�ۺ������ڸ�Ч�[���\�� 2023-03-22
- �|�A��Wʷ��ꖽ���/�������о��T�F� AFM: �p�Ӽ{���R�_���ڸ�Ч�[������ί����ί����װY���� 2025-03-17
- ��ۿƴ��Ʊ���Ժʿ�F�/����������n�}�M JACS���OӋһ�NAIE�ݭh���t��l��̽�����DNAzyme�������������ٰ�����ί� 2024-12-14
- �����˲ܷ����/���ϴ�W�������ڈF� AFM�������\�������ռ�����ί���Ħ��늹��ܼ���Ʒ 2024-12-07
- ��������ǵ��ΈF� ACS Nano�����Ӷ���@�o����λ�ۺ���ͺϼ{�������F�[���B�m�ߏ��ȹ��-���������ѭ�h�ί��ͻ��� 2025-08-01
- ����߿ƻ��W�WԺ�����۽����c������ JACS: �����͡��ø���{�ײ��� �� �I�������� 2025-07-20
- �칤����x/�R�w�R/���ƽ� Small����ˮ�˺�/�͜ع��fͬ�����[���ί� 2025-07-11
