�M�����^ȥʮ�����ж�N���Ϳ��[���������_�l�����o���Ժ�ȫ�����[�������Ļ��������R�����[���ί�����Ҫ��������Ŀǰ�����į�Ч߀�ܲ����롣���⣬�������Ƶ��[���h����TME��Ҳ�����ƻ����į�Ч�������[���Ͱl�D�ơ���ˣ�̽������Ч�T���[������ԭ�Ե��»������c����������ϵ�y�����DTME�����������ԣ��������F�������ί�Ч����
���|�W���鼚�����{�������|�ۯB�ͼ������B����Ҫ���������ѳɞ��µ�ˎ��W���c�����ڴ�����[��������̎�ڷ������ij��m���|�W������B���Ŵ���|�W�������T���[���������������⣬���[���Ѓ��|�W�����̶Ȯ��������r����λ�ڃ��|�W�ϵ�����ԭ��������ICD����־���}�W���ף�CRT�����D��������Ĥ���컯��ͻ������DCs������ˣ����ÿɷŴ���|�W������ˎ����MCRT�ڼ�������ı�¶�������������[������ԭ�Ե������x��
����������ڡ�one-for-all�������OӋ�ļ���\����ί����ܵļ{��ˎ�ﱻ�V���_�l����Ӱ���������[���ί���������������ט�������~�j���1G3-Cu�����ȿɌ��ٵ�������Bax�D�\�������w���T���[������������߀������Cu�M��MR�����⣬1G3-Cu�������w�ĝ��ړp�����܌�����һ�NICD��־�����������գ�ATP����ጷţ��Mһ������ICDЧ����
���ڻ���ˎ�������������������öȲ��ˎ��Ч�����ȱ�c�����Ѓ����dˎ������TME푑��{��ƽ�_���������ϲ�ͬ��ˎ������߯�Ч���ڱ���{��ƽ�_�У�푑��Ծۺ����z�����ڿ�ؓ�d��ˮˎ����LѪҺѭ�h�r�g�Լ�����ˎ��ጷŵȶ����Ъ��صă��ݡ�Ȼ�����w�ȵĶ������������ԕ���K�z�����[���еķe�ۣ�����б�Ҫ���z�������M���~��ķ���������������[���خ��ԡ����磬���������ӱ��Ժ�ͬԴ�����Եİ�����Ĥ��ʹ�{��ƽ�_��Ó�W���Ƥϵ�y�����ɲ����������[���еķe�ۡ����]�����[���ĸ�Ч�������ܕ������[�������������ߙz���c���ӱ��_���ӣ��������c���ߙz���c��ࣨICB�������Y�ό��������D�������Ƶ�TME���a���L�ڿ��[������ӛ��Ч����
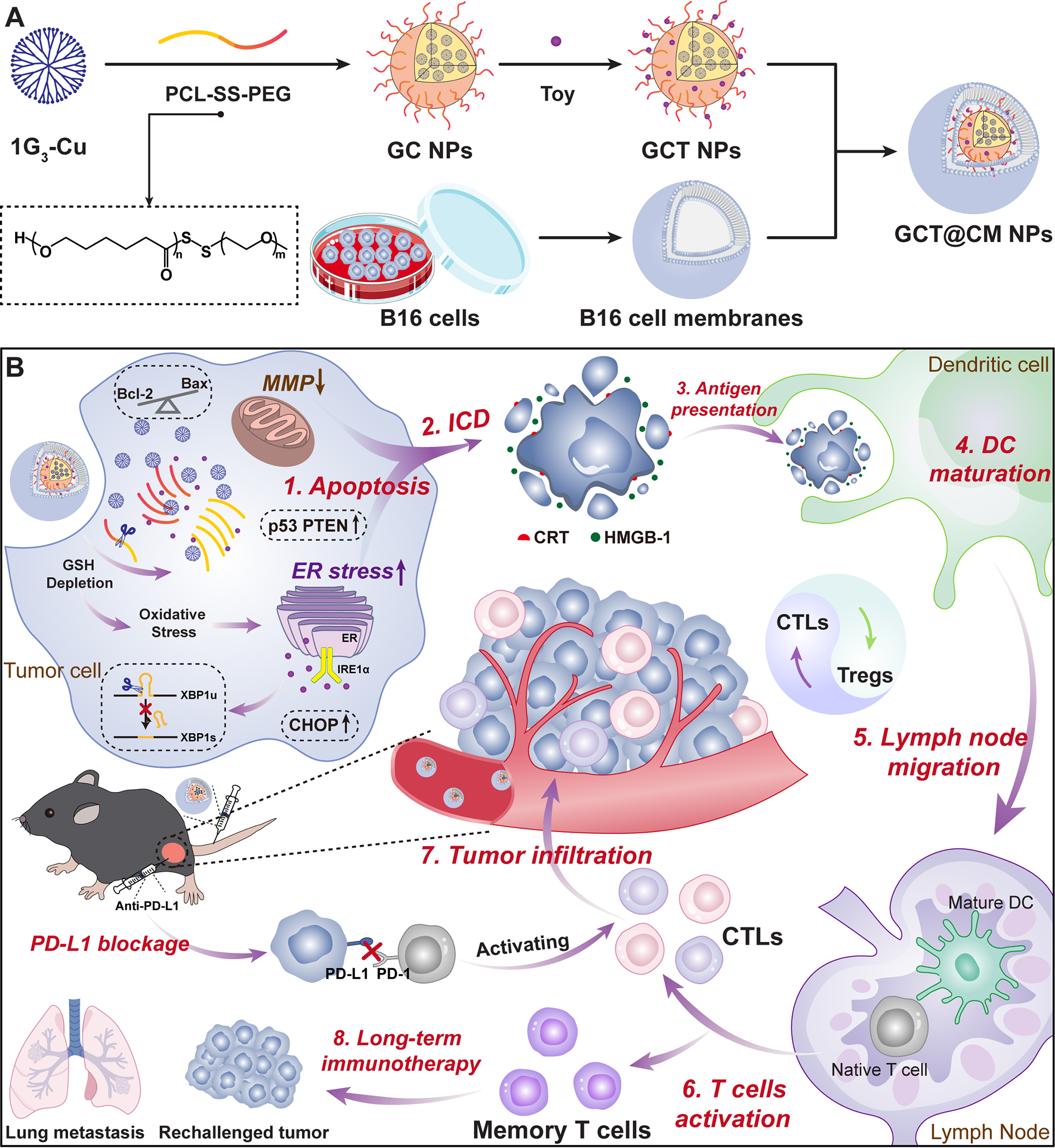
�D1. GCT@CM NPs�ĺϳɼ�����ʾ��D��

�D2.��A��GCT NPs��TEM�D��GCT@CM NPs�ģ�B��SEM�D����C��TEM�D����D��CD47���ı�����r����E�������ϵĿ��������������������ϵģ�F��ˮ����������G��늄ݣ���H��GCT@CM NPs��ˮ��PBS�Լ����B���е�����׃����������I����ͬ�l����GCT@CM NPs������׃������J����ͬ�l����Toy���۷eጷ�������

�D3.��ͬ����̎����A��B16������B��L929������ļ��������D����C����ͬ����̎��B16������RAW 264.7���������~Ԫ�غ��������D����D����ͬ����̎����B16������GSHˮƽ�����D����E-G��ROSˮƽ�����D����H��Toy�ڼ����ȵ����ÙC��ʾ��D����I-L����ͬ����̎����B16���������P����ı��_ˮƽ����M�����P����Western blotԇ�Y���D��

�D4.��A��1G3-Cu�ڼ����ȵ����ÙC��ʾ��D����B����ͬ����̎����B16�����Ⱦ����wĤ�λ׃�������D����C-D����ͬ����̎����B16����������r��ʽ��������E���������P����Western blotԇ�Y���D����F��B16�����c���M���Ϲ���������ICD�����̼�DCs�컯��ʾ��D����ͬ����̎�����ȣ�G��HMGB-1��ጷż���H��CRT���_��r�����D����I�����M���ϴ̼�DCs�컯����ʽ�����D��
�S���о��F���С���w�Ș�����B16Ƥ����ģ�ͣ�ͨ�^MR������C��GCT@CM NPs���w�Ⱦ����[�����Ӱ����Լ����L��ѪҺѭ�h�r�g�����w�ȿ��[������У�GCT@CM NPs������ѵ��[������Ч���������w���T���[�������l��ICD������ļ��������T�����M��TME���Mһ����GCT@CM NPs�cPD-L1���w��Anti-PD-L1����ʹ�ðl�F��Anti-PD-L1�����T�������[���������R�e������ʹGCT@CM NPs+Anti-PD-L1�MС����[���w�e��С���D5A-E��������ʽ�����l�F�����ί�ʹС��Ƣ�K���[��������CD4+��CD8+T���������@���������[����λTregs�ı����½����������Ƶ�TME�����D���������������ICD�cICB�����Ͽ���������Ч�����ߑ��𣨈D5F-K����

�D5.��A��С���w�����ί��^��ʾ��D����ͬ�����ί�14��ȣ�B�������[���w�e׃���D����C��С�������w��׃���D��14���ģ�D���[����Ƭ�ͣ�E���[�������������M���ί�14���F��Ƣ�K����G���[���M����CD8+�cCD4+T�������͵���ʽ���������D����H-I���[���M����Tregs�ı��_ˮƽ��������J��CD8+T�����cTregs�ı�ֵ����K���ί�����MС��Ѫ����IFN-�����_ˮƽ������

�D6.��A��С���w���[���������D�ƌ��ʾ��D����B-C�������ί�����MС��Ƣ�K��ӛ��T����������������D�����MС���������[����T�������ͷ�������E��CD8+�cCD4+T�����ı�ֵ����H�����MС���ί����D�ƌ��Y����
������֮��ԓ�о��OӋ��GCT@CM NPs�{��ƽ�_���ж������ݣ�1��������NPs��CM�@�������1G3-Cu��Toy���������öȲ������������ĸ����ã�ʹ1G3-Cu��Toy��TME��푑���ጷţ��Ķ�ͨ�^�����w�̓��|�W�����ɂ�;���T���[������������2��Toy�錧�ă��|�W�����Ŵ�����c1G3-Cu�T���ľ����w�����ϵK�fͬ���ã�����ICDЧ�����컯DCs����ļ�������M��TME��3��GCT@CM NPs�cAnti-PD-L1��ʹ�ã����a���L�����ߑ��������[���ďͰl���D�ơ����о��Ƃ��GCT@CM NPs�����ϲ�ͬ���ί����c�Ԍ��F���������������ί��ṩ���µ�˼·��
����朽ӣ�https://doi.org/10.1002/adma.202206861
- ��������ɭ/�����СԪ Nature���ӿ���������ˮ���z���ϼ���Ĥ����-���g���ǻֲ��������s��ˮ���z����{���[���ɼ�����̖ 2025-12-30
- ���_��Wꐴ�ȫ���ڈFꠣ��Y�����tˎ������Փ���������ڽ۹����ǵľ��ɼ���Ĥ�����{���d�w���ڰ�������Լ�ƽϢ���������L�� 2022-02-11
- �|�A��Wʷ��ꖽ����n�}�M��ACS Nano�������ɼ���Ĥ�����Ķ�ܼ{�����z����MR����������ԭλ�X�z�|�����ί� 2021-12-06
- �|�A��Wʷ��ꖽ��ڈF� AS������߀ԭ푑��͘�����Ӽ{�����zͨ�^���|�W�����Ŵ�;��ɼ����O�����F�����������ٰ����W�����ί� 2023-06-25
- ����������W�츣�����ڈFꠣ������_�h������������߀ԭ푑���֧����ه��������d�w 2019-03-21
- ���ݴ�W�����ƽ��ڈFꠡ�Acta Biomater.����ˎ����;ۺ���{���z�������[���LЧ�ί����о��ɹ� 2025-07-08
- ����W���������ڈFͺ�����Small���p�߷��Ӿۺ���{���z�������[���ί��ͽ��t����^��M������ 2021-12-08
