Ŀǰ�������Խ�Ĥ���R���ί������漰�ֲ������ص���Һ���p��ʽ��Ĥ��ֲ�������y��ͬ�r���Ⱦ���ơ��װY�{���c�M����������f�{��Ч�����c�����M�����o֮�g��ì�ܣ��о��ˆT�_�l��һ�N��ע��ķ����ͺϻ��|��ԓ���|�ɹ�푑����zԭ/���|��-������ż�CHB��ˮ���z�cԴ�Խ��S�غ͚����ǵĶ��̼�c��CC-CDs�����ɶ��ɡ�ע���CHBˮ���z����ԭλ�γ����Ҿ���ճ���ԵĽ��棻ͬ�r��CC-CDs��������x�Ӛ����ǽM�ְ����Ɖļ�������Ĥ�����l�]���S�������ļ{��ø�����ԾS�ּ����ȵ�����߀ԭƽ�⡣ֵ��ע����ǣ��������ˮ�Խ��S�أ�CC-CDs��ˮ����������4000�����ϣ��@���������俹����Ч�ܣ������F��ǰ��δ�е��p��Ч�����ڽӽ���ȫ���������ͬ�r��������98%���ϵļ�������ʡ������@�N���������������ԣ�ԓ�ͺ�ˮ���z�Mһ�����M�˾��ɼ�����������M2���͘O�����w�Ȍ��Y���@ʾ��ԓ������24С�r��ʹ�����d��������90%���ڵ�4�쌢����������ļ��������6�������ڵ�28��������91.8%���w�S����־�ͬ�r�֏���87.5%��ҕ�WĤ��̖���ȡ��@Щ�о��Y��ͻ�@��ԓ�ͺ�ˮ���zͨ�^���h���{�������F�o�۽Y���ޏ��cҕ�X���ܻ֏͵ąfͬ��������������y�ۿ����g�ṩ���²��ԡ�
�R���ϣ������Խ�Ĥ���ί������R�������Θˡ����α�����Խ��ƿ�i���F�е��ί�������Ҫ��ه�ֲ��l���μӿ����ص���Һ�����@������ˎ���v���r�g�̡��������öȵͶ����¸�Ⱦ���ͣ��������ذY���ߣ��p��ʽ��Ĥ��ֲ�m���ؽ��۱����s�O�����l���g�p�����P�ęCе�̼��������װY���������ų⡣����������ǣ���һ���ί��ֶ������ʧ�ˣ������������ܼӄ����������������p�������μ��������ޏ����y�ԑ������s���װY�h������ˣ��_�lһ�N��ͬ�r���ԭ�w����������װY��B�p���{���c��Ĥ�M��ԭλ������ȫЧ�ޏ��wϵ���ѳɞ��ۿ������t�W�I��ؽ��ͻ�Ƶ��n�}��
���ڣ��Ĵ���W�����t�W���̌WԺ/���������t�W���Ϲ��̼��g�о����ČO�o/���t�ɈF�ᘌ������Խ�Ĥ���ί��в�ԭ�w�����c�װY�p��������R����������ˮ�ᷨ���������c���S��ǰ��w�D���鎧��늺ɵ�̼�c��CC-CDs�������F���ø�����������c�������ܵ���Ч���ϡ��о��F�����ͨ�^�ܶȷ�����Փ��DFT���ķ���ˮƽ��ʾ��̼�c�Ĵ��C������C����ǻ�������ه���x���Կ����C�ƣ��˷��˂��y����ϵ�y�������������o��e�p���ľ����ԡ��S�Fꠌ�ԓ�����ø���Ե�CC-CDs��������zԭ/���|����|�У�������һ�N�����p��ճ�������c�r�Յfͬ�ί�Ч���ďͺ��øˮ���z��CHB@CC����ԓˮ���z���Hչ�F�����������ȡ��M��ճ��������������ROS����������������T�����ɼ����������ͣ�M2�ͣ��O�����������m�ü����Խ�Ĥ��ģ���У�ԓ�wϵ���F�˄���ļ��r�ܷ��c���ڿ��ך�������ͨ�^���������ɡ�������Ĥ�M���o�����ϣ��ɹ��֏�������Ĺ����̖�D�����ܡ��@��о��阋����ȫ����Ч�����Ϳ����{���tˎϵ�y�ṩ����Փ������Ҳ���Ĥ�p������h���{���c���������ṩ���µ��R���D��˼·��
2026��2��14�գ����P�о��ɹ��ԡ�Enzyme-Mimetic Hydrogel Balancing Antibacterial Activity and Cytoprotection for Corneal Regeneration in Bacterial Keratitis�����}�l����֪���W�g�ڿ���ACS Nano���ϡ��Ĵ���W�����t�W���̌WԺ/���������t�W���Ϲ��̼��g�о������DŽP��ʿ�����µ�һ���ߡ�ԓ�о��õ��ˇ�����Ȼ�ƌW����ί��֧�֡�

�D1 ���CHB@CCˮ���z�ί������Խ�Ĥ��ʾ��D�����{�����ښ��缚�����{���װY�����M��Ĥ�M���ޏͷ���ąfͬ���ã��Ķ����F��Ч�������ί���

�D2 CC-CDs���w�⿹�������u�r���C���о���

�D3 ����ճ����CHB@CCˮ���z���Ƃ��c������

�D4 CHB@CCˮ���z�ڽ��Sɫ���������Ⱦ�Ľ�Ĥȱ�pģ���е��w���ί��u�r��
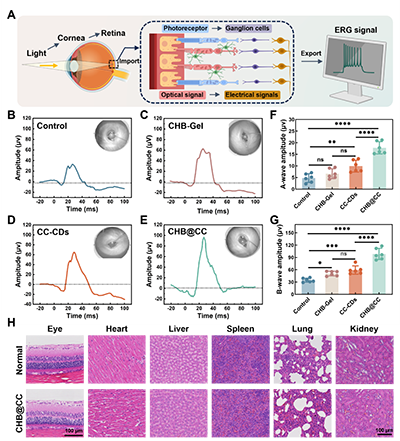
�D5ͨ�^ҕ�WĤ늈D��ERG���u��ҕ�WĤ��-���̖�D�����ܣ����淴ӳ��Ĥ�p���ޏ���r��
ԓ�����LjF����ڷ������|�OӋ�ί��۱������I���ϵ���Mչ֮һ��ᘌ����s���ۿƲ����h����ԓ�F������ڽM�������t�W�����zԭ���ס���Ĥ����Ȼ������|����ģ�ͨ�^����ˮƽ�Ĺ��ܻ�����c�����Y���������_�l��һϵ�о߂�߶������������c�h���{���������T�����ޏͲ��ϡ�����������Fꠘ�����ȫ��λ���ۿ��ί���ꇣ����ȣ����zԭ���מ��ʯ�����Ƴ����з����Ӡ�Y���������ʼ��������W���ܵ��˹���Ĥ�����龏���R�����w�T���ṩ����·����Small 2024����ᘌ����y�p�ϲ��l�Y����һ���|���ܾ��ޣ��F��_�l�˼�ԭλճ������������������һ�w�ďͺ�ˮ���z�����F�˼����Խ�Ĥ�ĸ�Ч�ί���ACS Nano 2026�������⣬ͨ�^����Ĥ���|�����϶�ø�����i��̼�c����Ч�����˽�Ĥ�A�����������Ѫ���c���γɣ�Acta Biomaterialia 2025�������۵����I�Fꠘ������zԭ/�h������ע���f��ϵ�y�����F���������c���������ąfͬ�f�ͣ���ҕ�WĤĸ���������ί��ṩ���²��ԣ�Acta Pharmaceutica Sinica B 2025����Ŀǰ��ԓ�F����e�O̽�����Ϲ��ܻ���ҕ�p���ޏ��е�ǰ�ؑ��ã������ڴ��츲�w�۱����۵�ȫ���ί��wϵ��
ԭ��朽ӣ�https://pubs.acs.org/doi/10.1021/acsnano.5c22118
- ꃿƴ����W������/�h������ JCIS�����������������Ժͷ������ܵĶ�������ۻ��ɳ��mʳƷ���b 2025-04-27
- �����Ҹ��W�_ꖳ��F� Adv. Compos. Hybrid Mater.�������ǻ��p�W�jˮ���z�Ę����c���Լ��䏊�������� 2023-11-11
- �㽭��W��ε豽��ڈF� AM�����͟������}����������PET�U�ϵ������������� 2023-04-30
- �ȴ���� ��D���ڡ������Ӣ������ ACS Nano���������T������̖�Ă��b���g�ί������Խ�Ĥ�� 2025-09-17
- ����������n�}�M��Adv. Sci.���C������������ڽ�Ĥ�����еđ��� 2025-01-02
