������ȫ���������͚�������Ҫԭ��֮һ���AӋ��2050�꣬�����ߔ������_13.1�|����ǰѪ�ǹ�����Ҫ��هÿ�ն��Ƥ��ע���ȍu�ء�Ȼ�������s���ճ��������ʹѪ�ǃ������Ə��s�����������ȍu���{��Ѫ��ˮƽ�į�Ч����������Ƥ��ע��o���ߎ������ص��ί�ؓ���͉�����Ŀǰ�R��ʹ�õĶ�N�LЧ�ȍu�������L����Ч�{��Ѫ��ˮƽ������ע���l�ʣ��������ڲͺ�Ѫ��ؓ�����˺��Գ��m�l�]���������ڵ������˵�Ѫ���L�U��
�����x�����n�}�M��ǰ���о��У�������ԃ������ﰲȫ�Եľۇf����ģ�M��Ȼ���ģ������Ե،��F�˻��ھۇf�����ǼܵĹ����Զ���ģ�M���l�F�˾��ж�N������Եľۇf�������Է��ӣ�Angew. Chem. Int. Ed. 2020, 59, 6412��VIPՓ�ģ�ESI�߱�����Angew. Chem. Int. Ed. 2022, 61, e202200778��VIPՓ�ģ�J. Am. Chem. Soc. 2023, 145, 25753��JACS Spotlight�������о��Mһ������OӋ����������������Ժ��c�ȍu���γɏ��o��������늺ɾۇf�����ۺ��������Ƃ䳬�LЧ������푑����ȍu���Ƅ����²��ԡ��ھۺ����������p�һ��Fȡ���������c�ȍu��ͨ�^�o������γɏͺ��ͨ�^���I���}���p�������c�ȍu���γɸ�������ã��@�����ߺ��������ȍu��ؓ�d�������D1�����Mһ���ھۺ��������4-�Ȼ�-3-�������ᣨFPBA�����F������푑����ȍu��ጷš���1����������ģ���У��δ�Ƥ��ע��ɾS�������i����Ѫ�dz��^192С�r�����O�ٳ��F��Ѫ���͵�Ѫ���¼����D1�������о��鳬�LЧ������푑����ȍu���Ƅ����_�l���R��������Ѫ�ǹ����ṩ��һ�N�O�ߝ������x��
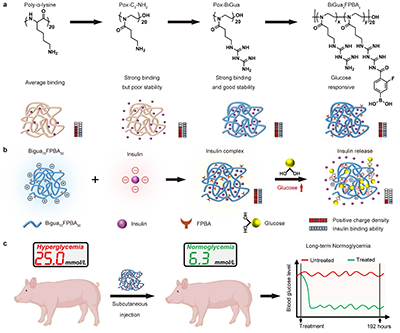
�D1. ������푑��;ۺ���-�ȍu���Ƅ����OӋ���ԡ�
2025��10��23�գ�ԓ�о��ɹ�����Poly-(bis(guanidinium)-oxazoline)-Insulin Complex Exerting Long-Acting Glucose-Responsive Insulin Release in Mice and Minipigs�����}�l����Journal of the American Chemical Society (DOI : 10.1021/jacs.5c12605)��

�D2. ������푑����ۺ���ϳ��c�w�������������о�
���о�ʹ��������������������l��ͨ�^��x���_�h�ۺϷ����ϳ���L20mer�ۇf�����ۺ��ȥ�����o�����M���p�һ�����õ��p�һ�����(2-�f����)��Pox-BiGua�����D2a�����Mһ��ͨ�^N-�u��������������NHS�����c�p�һ��F�����ķ������ϳ������������ᣨFPBA�����Pox-BiGua��BiGuaxFPBAy, x + y = 100%, x = 50, 60, 70, 80, 90, 100%������Ѫ�ͺͼ��������о��Y��������BiGuaxFPBAyϵ�оۺ��������:���ʬF�^�Ͷ��ԣ�HC10��IC50ֵ������400 ��g/mL�����Y������BiGuaxFPBAyϵ�оۺ���������õ����������ԣ��D2e, 2f����

�D3. ��ͬ�ۺ�����ȍu�ؽY�������c������푑�ጷ��о�
�ȍu��ؓ�d���Y��������FPBA���ܻ���BiGuaxFPBAyϵ���ۺ������F��92.7%��97.1%���^���ȍu��ؓ�d�ʣ��D3c�����������cBiGuaxFPBAy�ۺ�����FPBA�ĽY�ϕ�������늺��ܶȣ��Ķ��p���ۺ����c�ȍu���g���o�������������ȍu�؏ďͺ�����ጷţ��D3d����������푑�ጷ��Y������BiGuaxFPBAyϵ���ۺ����c�ȍu���γɵ��ȍu�؏ͺ�����������õ������ǝ��푑�ጷ��ȍu�ص��������D3e��3i�����ۺ�����FPBA��ȵ����ӕ�������늺��ܶȲ���������ǽY�����������¾ۺ���-�ȍu�؏ͺ��ﷀ�����½����ȍu��ጷ�ʧ�ء��C�����������Ժ��ȍu��푑��ԣ�������BiGua70FPBA30���郞�x�ۺ�����c�ȍu���γɵ��ͺ������F���߷����ԡ��`���ɿص�������푑����Լ��������������ԣ��D3b��3g��S18��S21����
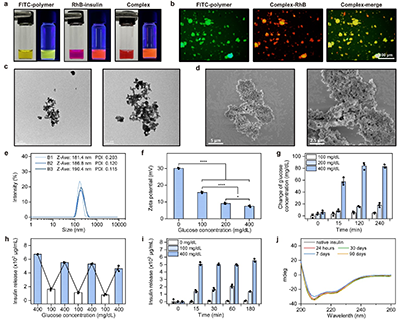
�D4. BiGua70FPBA30-�ȍu�؏ͺ���ı��������L�ڃ��淀�����о���
ͨ�^��������ɹ��أ�FITC����ӛ��BiGua70FPBA30�c�_����B��RhB����ӛ�ȍu�صğɹ��λ���Mһ����C���ȍu���c�ۺ���ďͺ����ã��D4a, b�����ӑB��ɢ�䣨DLS���Y���������Ƃ���ȍu�؏ͺ���������s��200 nm���D4e������������@�R��SEM����������@�R��TEM���Y���������ͺ����ɴ����{���w���ۼ��γɣ��D4c, d��������ɢ��Y�������������Ǻ��ȍu�صĿ��ٔUɢ�c���Q�����λ�y���Y���������ȍu�؏ͺ�������λ�y��ֵ�s��+30.0 mV���D4f���������ǽY�ό������ȍu�؏ͺ���늺��ܶȽ��ͣ��D4f������ͺ���Ҹ�Һ�м��������Ǻ������ǝ�������½�����������п��ٽY�������Ǻ�ѭ�h���}�_ʽ�ȍu��ጷ��������D4g, h������4��C����90���ԓ�ȍu�؏ͺ����Ա���������푑�ጷ����ԣ��D4i�������ďͺ�����ጷŵ��ȍu���Ա���������Y����������ԣ��D4j����

�D5.�ȍu�؏ͺ�����w�Ȝ������Լ�BiGua70FPBA30�ۺ�����w������ֲ��о���
������С��ģ�����u�����ȍu�؏ͺ������ȍu���c�ۺ���Ĝ������Լ�����ֲ����w�ȟɹ����Y���@ʾ��RhB-�ȍu�؏ͺ������������@���������x��RhB-�ȍu�ء�BiGua70FPBA30������ֲ��о��Y���l�F��ע����4С�r��BiGua70FPBA30��Ҫ�ֲ��ڸ��K���I�K���D5d����ע���4С�r��96С�r���g��BiGua70FPBA30���K���е��ɹ���̖��u�p�����D5d�����ί�96С�r��С�����Ҫ�������H�^�쵽���ɹ⣬����BiGua70FPBA30�ѱ���u������D5d����BiGua70FPBA30������^���c�ȍu�؏ͺ�����w������ͬ������Ҫͨ�^���K���I�K���x���D5e��5i����
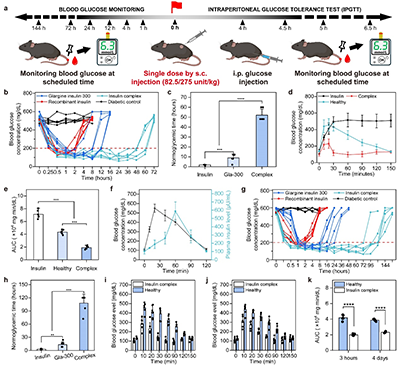
�D6.�ȍu�؏ͺ����ί�1������С����w�ȯ�Ч�u����
�ȍu�؏ͺ�������������أ�STZ���T����1������С��ģ���б��F����ɫ���ί�Ч�������Y��������Ч�ȍu������82.5 U/kg�ȍu�؏ͺ���ɾS������С������Ѫ�dz��^48С�r���@���L��ͬ�Ȅ����µ���Ȼ�ȍu�أ��s2С�r�����LЧ�ȍu�ظʾ��ȍu��Gla-300��9С�r�����D6b�����ͺ����ί��M��40%��С�����ί���60С�r�Ա�������Ѫ�ǣ�������С��Ѫ��ֵ�����ڳ�ʼˮƽ�������ͺ�����60С�r���Գ��m��Ч���D6b, c������ǻ����������ԇIPGTT���Y���������ͺ����ί��M��Ѫ����30��犃Ȼ֏�������ˮƽ�����ڽ������սM120��犵Ļ֏��ٶȣ��D6d, e����Ѫ���@�����ߵ�ͬ�r���SѪ�{�ȍu�صĿ����������D6f������Ч�����ί����Y���������ȍu�؏ͺ����܌�Ѫ�ǾS�������������ȳ��^120С�r���D6g, h������δ�l����Ѫ���¼����s50%�ďͺ����ί��MС���ڽoˎ144С�r��Ѫ���Ե��ڳ�ʼˮƽ�������ͺ������Ч�Կɳ��m���^6�죨�D6g�������ί���3С�r��4���M����IPGTT���Y���������ͺ�����Ѹ�ٌ���ֵѪ���{��������ˮƽ����څ���c����С��һ�£��D6i��6k����

�D7.�ȍu�؏ͺ����ί�1������С���i���w�ȯ�Ч�u����
�ȍu�؏ͺ�������������أ�STZ���T����1���������R�i�б��F����ɫ���ί�Ч�����ͺ����ί�������С���i��Ѫ���@�����ߕr�����SѪ�{�ȍu�صļ����������S�����½�������ԓ�ͺ����ڴ��̈́�����ͬ�Ӿ߂������������푑����ԣ��D7b�������m�����DZO�yϵ�y�B�m�O�yѪ���Č��Y���������R��ʹ�õĸʾ��ȍu�صĿ���Ѫ��ˮƽ�����r�g�����^24С�r���D7e�������ȍu�؏ͺ����ί�����Ѫ��ˮƽ�����r�g�_168С�r��156С�r��192С�r���D7f����ԓ�ͺ����������ί����g��Ѫ�ǾS��������������50-200 mg/dL��������Ѫ���͵�Ѫ�����ӿɺ�����Ӌ���D7f�����@һ�Y�����H�@ʾ��ԓ�ȍu�؏ͺ���Խ��Ѫ�ǹ�������������ȫ�����R�������LЧ�ȍu�����ܵ��A�ڡ������ί�180С�r��1̖�i����168С�r��2̖�i����216С�r��3̖�i�����������i��Ѫ����δ��������ʼˮƽ�������ͺ����ܳ��m�{��Ѫ�dz��^216С�r���D7f����

�D8. BiGua70FPBA30�ۺ��PBiGua70FPBA30-�ȍu�؏ͺ�����w�ȶ����u����
BiGua70FPBA3�ۺ�����ȍu�؏ͺ�����С���w�ȱ��F���õ����������ԡ����؏ͽoˎ�������о��У�Ƥ��ע��BiGua70FPBA30�����ȍu�؏ͺ����7���14�죬С���w�ؾ��������L���D8b����ѪҺ����ָ�ˣ��D8c��8i����ȫѪ����Ӌ���cPBS���սM��Ⱦ��o�@��׃����ע�����7��͵�14�����Ҫ�K�����M���W�����Y��������BiGua70FPBA30�����ȍu�؏ͺ���δ���F�����@���ԣ��D8j, k����ע�䲿λƤ�w��Ƭ�M���W�����Y���������B�mע��7���14��������������������w�S���̶ȿɺ��Բ�Ӌ���DS33�����@Щ�Y����ͬ�C��BiGua70FPBA30�����ȍu�؏ͺ�����������w����ȫ�ԡ�
�A�|������W���ϿƌW�c���̌WԺ��ʿ����껖|��ԓՓ�ĵĵ�һ���ߣ��A�|������W�����x������Փ�ĵ�ͨӍ���ߡ�ԓ�о��õ��ˇ�����Ȼ�ƌW����ί����������W�c�ӑB���W������ǰ�ؿƌW�����Ȼ�����Y����
Փ��朽�: https://doi.org/10.1021/jacs.5c12605
