���I����ͨ�^����[����ѪҺ�����Z������ĠI�B(y��ng)���|(zh��)���������Ǻ����⣬�������[�������L�ʹ�Ȼ�������I�������ڳ־��Բ���[���װl(f��)���Ͱl(f��)���D(zhu��n)�ƵĹ���ȱ�c����һ���棬���y(t��ng)�Ļ��W�ί����߹�W�ί�����Ҫʹ�û���ˎ���߹����@ЩС���Ӷ������|(zh��)��ʹ���^���Пo�����ⶾ�����õĮa(ch��n)�����������M���ĕ���ɲ�����ēp������ˣ�ؽ���_�l(f��)�µ��[���ί���ʽ�Խ�Q���y(t��ng)�[���ί��^���еĆ��}��

���ڣ����ϴ�W���|���������F����һ�N�o��ˎ��������ۺ���W(w��ng)�j(lu��)��IPN��ˮ���z�����[�����I�ί����ԡ����Üض�푑������ɻ��ۺϵ�ˮ���z�����z���^�����տs�����ă�(n��i)�����;ֲ��ߜ��ğ�Ч�������[��Ѫ�ܵĉ��s���[�������ڹ�ͬ�γɵąf(xi��)ͬЧ�����Ԍ��F(xi��n)�����[���ί���ʹ��N-��������ϩ����(NIPAM)�Ĝ������ԣ���(y��u)���������R��ض����w�ط�����(n��i)��ʹ��NIPAM�Ě��I�Ɖĺ�ጷŵğ��������±���������̶������ɻ����±�����T�����w�ۺϲ�����ԭλ��Ч���Įa(ch��n)�����w������ˮ���z�����z���^���о���58.5%���տs�ʣ��w��(n��i)����C���@�Nˮ���z���@������Ѫ���ܶȡ��T���[��ȱ�������_�����I�����[��������Ŀ�ġ��Y(ji��)��ˮ���z��ԭλ��Ч���T���������������F(xi��n)��Ч�[�����I�M���ί����˲��Ԟ��_�l(f��)�o����/�⯟ˎ�����I�����ṩ����˼·��
��D1��ʾ��������(g��u)������ע���IPNˮ���z������Ҫ�Ƀɂ����ܽM�֘�(g��u)�ɣ���푑��ԽM�֣���A�z�����c�ᯟ�M�֣���B�z������ͨ�^���_�{(di��o)��NIPAM�ı�������A�z���R���ۺ��ضȿ�����34.3����A�z��NIPAM�Ě��I�Y(ji��)��(g��u)�ڸ�������R��ض��r���Ɖģ�ͬ�rጷş������@Щ����ʹ����������Ě����������CS-NI�������̶������ɻ����ጷţ��Ķ����F(xi��n)A�z�Ĝ����ۺϡ��@һ�^��ͨ�^���ɻ�̽ᘺ����������EPR�������C�����Mһ���о���B�z��IPNˮ���z��ԭλ��Ч������D2��ʾ��B�z��IPNˮ���z�S����ϩ�����ı������ӣ�����ߜضȷքe�ɵ��_95���47�档����IPNˮ���zͨ�^����ע��A�z��B�z�γɣ������ɻ��Y(ji��)�ϵğ�Ч�������Ɖ������M�����m�������[��ԭλ�ᯟ���S��IPNˮ���z��(y��u)�������W���ܣ����������ϡ�ճ�����ȡ�����͉��s���ȣ�ͨ�^��׃�ȷ�ʽ�õ��C�����D3�����������w��ģ�MѪ���Č���У�A�z��IPNˮ���z�����z���^���о����и��տs�ʣ��քe�_��42.5��58.5%���D4�����ڼ����ͼ�����ˮƽ����У��@�NIPNˮ���z���������õ�����Ч�����D5��������ڄ���ˮƽ��ʹ�ö����ղʳ����g(sh��)���C����IPNˮ���z��Ѫ����l(f��)�����z���������[���܇���Ѫ�ܣ���Ч���ѪҺ���I�B(y��ng)���o���_�����I������Ч�����D6�����Y(ji��)��IPNˮ���z��ԭλ��Ч����IPNˮ���z�@�������[����Ѫ���ܶȣ��T���ֲ�ȱ���ʹ��M�[��������������K���Ѓ�(y��u)�����[�����L����Ч����
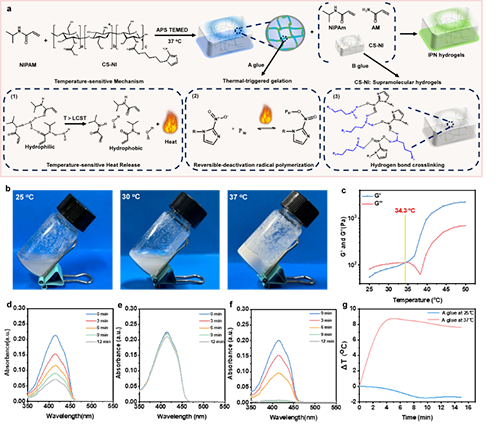
�D1��a��IPNˮ���z�Ƃ�ʾ��D��NIPAM���w��LCST�Ϯa(ch��n)���������^�̡���LCST��ԭλ�ۺ�IPNˮ���z����b��A�z��25��C��30��C��37��C�����z���О�Ĕ�(sh��)�a��Ƭ����c��A�z�Ĝض���ه����׃�������������z���ضȶ��x�郦��ģ����G�����͓p��ģ����G�������Ľ��c��ͨ�^�y��1,3-������������ૣ�DPBF���壬��25��C�����ɻ��a(ch��n)����d��CS-NI+APS+TEMED����37��C�®a(ch��n)����e��CS-NI+APS+TEMED����f���քe��25��C��25��34��37��C��APS+TEMED��CS-NI+APS+TEMED��EPR���V����g����A�z�Ĝضȷքe��ߵ�25��34��37��C��

�D2��a��37��C��A�z��B�z��IPNˮ���z�Ē�����R��SEM���D��b���ض������ͣ�e��B�z�ğ�D��(AM@NIPAM@CS-NI��0.3 mg mL-1 AM����B''''�z(AM@CS-NI��0.3mg mL-1 AM������c��A�z��B�z�����z���r�g����d��ʹ����IPNˮ���z��25��C��37��C�����z���О�Ĕ�(sh��)�a��Ƭ����f��IPNˮ���z��37��C�²�ͬ�r�g�Ĝض���������g��IPNˮ���z��25��C��37��C�²�ͬ�r�g�ğ�D��h��A�z��B�z��25��C�µ�ע��������A�z��B�z�քe�Á����{Ⱦ�Ϻ͙����S�������S��Ⱦ��Ⱦɫ��
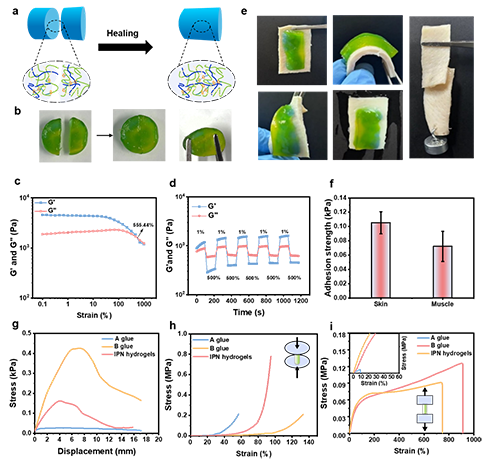
�D3��a��IPNˮ���z�������ܵ�ʾ��D����b��IPNˮ���z�����О�ĈD����37���½��|20��犺ɂ����x�ĉKʹ������ˮ���z���ϡ���c����37��c��IPNˮ���z��0.1%��׃���赽1000%��׃����d���ڸߑ�׃��500%���͵͑�׃��1%��֮�g�����M����݆�A�S��׃ѭ�h(hu��n)��IPNˮ���z��׃���ܵĕr�g��׃����e���@ʾˮ���z���iƤ��ճ�������͙Cе협��Ե���Ƭ������ˮ���z�ڏ�����׃���¾o�o��ճ����Ƥ�w�ϡ�ֵ��ע����ǣ���ʹ����ˮ�_ϴ�r����Ҳ���ι̵��B����һ�𣬛]���κ�Ó�����ѡ���f��IPNˮ���z��Ƥ�w�ͼ����ճ��������g��A�z��B�z��IPNˮ���z��Ƥ�w��ճ�����ȡ���h��A�z��B�z��IPNˮ���z�ĉ��s����-��׃������
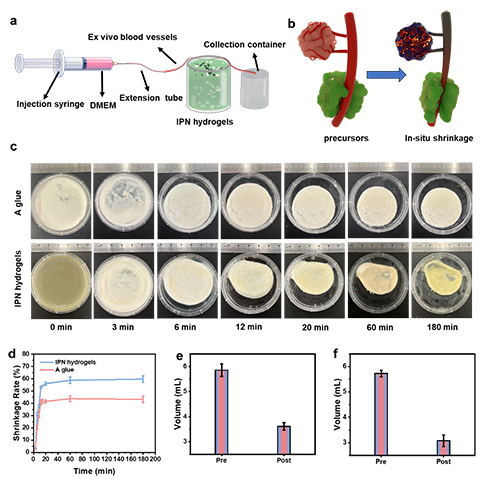
�D4��a������Ѫ�������z�տs����ă�(n��i)�����D��Ѫ�ܣ�����Ѫ�ܣ���(n��i)��1.00mm���x�w�]��Ч���Č���^��ʾ��D����b���w��(n��i)ʾ��D���f��Ѫ�������z�տs�T���ă�(n��i)��������Ѫ���]������c��A�z��IPNˮ���z��37��c���տs��ͬ��犵���Ƭ����d��A�z��IPNˮ���z��37��C�µ��տs�ʡ�DMEM�ڣ�e��A�z�ͣ�f��IPNˮ���z���z�ۺ�֮ǰ����֮���ң����^С���}��ϵ�y(t��ng)��

�D5��a��L929��������ԇ�ͣ�b��0С�r��12С�r��24С�r�Ķ���������̓����ʾ��ʼ���ۅ^(q��)��c��A�z��B�z��IPNˮ���z��L929������24С�r�����µļ�������ʡ���d��ʹ���}�S�G��AM/PIȾɫ��A�z��B�z��IPNˮ���z��4T1�����Ļ�/��������M�Мy������e�������B(y��ng)�����ʹ���}�S�G��AM���Gɫ����PI���tɫ������IPNˮ���z̎����4T1�������w�M�л�/������ʜy����

�D6��a��ͨ�^�տs�(q��)���]��Ч���ߜ��M�����I�ί���ԭλע��IPNˮ���zʾ��D����b��SD�����}�܇�ע��A�z����Һ��CDFI�D���e�Ƿքe��ע��ˮ���zǰ���Ĕz��CDFI�D�����а�ɫ���^��ʾ�������}��Ѫ�ܡ���c��ע��IPNˮ���z�ĺ���С��ļt���D��d���քe��(j��ng)�vG1�����ա�G2:CS-NI��G3:A�z��G4:B�z��G5:IPNˮ���z��4T1����BALB/c������[���w�e�S�r�g׃����n=5������e��ͨ�^ϵ�y(t��ng)�oˎ�M���[�����ʵ���Ƭ����f���ί���ɺ��[���M����Ƭ��HIF-1����VEGF��CD31�����ߟɹ�D���[���У�g��CD31����h��VEGF�ͣ�i��HIF-1���Ķ���������
���P(gu��n)�ɹ�����Thermal-Triggered Polymerizable Hydrogels with Localized Hyperthermia for Shrinkage-Driven Starvation Therapy�����}�l(f��)���ڡ�Advanced Functional Materials���ϡ����ϴ�W�����t(y��)�W���̌WԺ�����µ�һ��λ�����ϴ�W�о������������µ�һ���������|�������ں��ï�A�����ڞ�����ͨӍ������ԓ�о��õ�������Ȼ�ƌW�����Ŀ��52203160, 52362006, 32360238�����������ݞ��Ƽ���ݼӢ�˲��Ŀ��SKJC-JYRC-2024-34, SKJC-JYRC-2024-33���Y����
Փ��朽ӣ�https://doi.org/10.1002/adfm.202512839
- �����ֿƴ��䏩/�ǫI�¡�����������ꐝ�/Ф�i��Nat. Commun.��: �nj��Q�H��ˮ���|(zh��)�Y(ji��)��(g��u)�(q��)�ӿ���ˮ�Uɢ - �s��ˮ���z���F(xi��n)��Ч���ˮ�ռ� 2026-04-02
- ����i Adv. Mater.����x��-�л��i�Y(ji��)��(g��u)��ע�䌧�ˮ���z - ��(g��u)����(w��n)���ĽM��-������Ә��� 2026-03-21
- �Ͼ���W����/��� AFM�����ڸ�Ч��(w��n)�����l(f��)��s�ķ������w�����������ˮ���z 2026-03-20
- �A�|������W�������[�����I�����о��Ы@��Ҫ�Mչ 2017-02-16
�\���P(gu��n)ע�߷��ӿƼ�

- ���a(ch��n)���h�Ӱ�������^��PMEC...
- ��ʲô2026����ИI(y��)���h����...
- ��ˎ����Ч����������PMEC C...
- 2026����ߌ��Ї�����Ұl(f��)չ...
- �����I(l��ng)Ʊح300+���h��I(y��)�R��...
- �P���Ж|�����L���Ѓx�����{...
- �f����Ŀ �ذ��_�֣�2025�C...
- ICIE���H(�V��)Ϳ�Ϲ��I(y��)չ�[...
- �_չ�ڼ����ۄ�������朄�δ...
- 9������Ҋ���£�AI�(q��)��+���a(ch��n)...
- �P(gu��n)���e�k�ڶ�ʮ�����Ї����H...
- �۳Ǵ�Steven Wang���ڡ��^...
- �����ֿƴ��䏩/�ǫI�¡���...
- ���������ƾ��_���ڡ������i...
- �A�ƴ��T�ض����ڈF� Macro...
- �����������/���t(y��)������� ...
- ������ꐏ����ڈF� Matter...
- �������մ�/���� AFM���w�S...
- �A������߅�������w�i������...
- ���A��W���r�F� AFM���U�f...
- ���������x�����ڈF� Nat. ...
- �A�����������塢�V�|������...