��ˎ��Ծ���Ⱦ�����ʸߣ��ҽ�50����δ����e���������������ؽ���_�l���Ϳ���ˎ�������@һȫ���l�����{�����������ģ�HDPs������ģ�M�����䲻���T����ˎ�Եă��c����ҕ��O��ǰ���Ŀ���ˎ����Ⱦ���xˎ������w�ȭh�������ܕ��c����������ؓ늺��������ӵȰl�����خ�������ã��M�����l��Ѫ���Ե����}����ˣ��OӋ�����Ч�w�Ȼ��Ժ��������������Ե�HDPģ�M������������������ˎ������Ⱦ�ί�������Ҫ���x��
���о��У������x�����n�}�M�������Ⱦ����ԭλ푑������ۺ���ǰˎ�����ԡ�ԓ����ͨ�^2,3-�����R��������ۺ����朰�������������늺ɣ��Ķ��@��������������Բ����LѪҺѭ�h�r�g���ڸ�Ⱦ����������h���У�ǰˎ�ɱ�����֏���늺ɣ����F���ʿ����Ͳ�����λ���������⣬�@һ�OӋ߀�@���،���HDP�����������w�ȑ����������Ɍ�ԭ�����ԵȆ��}���Ŀ����������D���鰲ȫ��Ч���ί����xˎ�������������ˎ�����_�lЧ�������ڴ˲����OӋ��HDPģ�M�ۣ�2-�f������ǰˎ��Ƥ��ē�[�������������p�ٴ��ȸ�Ⱦ���I�K��Ⱦ���β���Ⱦ����Ĥ�ȶ�N�����Ⱦģ���о�չ�F���������ί�Ч�������L��ʹ��δ�T����ˎ�Ԯa����ԓ�о����OӋ���Ϳ���ˎ����ί���ˎ�����Ⱦ�ṩ�˄��²��ԡ�

2025��6��4�գ�ԓ�о��ɹ��ԡ�A host defense peptide-mimicking prodrug activated by drug-resistant Gram-negative bacterial infections�����}�l����Science Translational Medicine�������x��������������Sci. Transl. Med. 2025, DOI: 10.1126/scitranslmed.adl4870����
��ˎ������Ⱦ����l���ʺ������ʸ������ɞ����{��������������ش��l�����}���������m����Ծ�����ֵ��R�����}֮һ��Ҳ����ˎ�Ը�Ⱦ��������Ҫԭ��Ȼ����������Ծ����и߶Ȳ��ɝB����Ĥ���ϣ�����ᘌ���Ծ��ĺ��xˎ�������^�����ҽ�50����δ�ܰl�F��e�����ء���������������ģ�M�������V�V�������Ժ������T�������a����ˎ�ԵĪ����ݣ��ǽ�Q��ˎ����Ⱦ����ǰ�����ί����xˎ��֮һ��Ȼ�����ڏ��s���w�ȭh���У��@ЩHDP��Է��ӿ������c�t���������ж���x��Ĥ�Y�������������Լ�Ѫ�嵰�ȶ���x�Ӵ���Ӱl�����خ�������ã��Ķ������w�ȿ������Խ��͡���Ѫ�����ȡ��@һ�L�ڴ��ڵ��ƌW��������ʹ�OӋ��߸��w�Ȼ��������������Ե����Ϳ���ˎ����ί�ȫ������ˎ������Ⱦ��
�����x�����n�}�M��ǰ���о��У�������ԃ������ﰲȫ�Եľۇf��������������������I�D������朣�ģ�M��Ȼ���ģ������Ե،��F�˻��ھۇf�����ǼܵĹ����Զ���ģ�M���l�F���w�����Ч����ˎ��������ˎ����ľۇf�������Է��ӣ�Angew. Chem. Int. Ed. 2020, 59, 6412��VIPՓ�ģ�ESI�߱�����Angew. Chem. Int. Ed. 2022, 61, e202200778��VIPՓ�ģ�J. Am. Chem. Soc. 2023, 145, 25753��JACS Spotlight��Nat. Microbiol. 2024, 9, 1325, ESI�߱����������о������һ�N ����푑������ۺ���ǰˎ�����ԣ���ʹ�þۣ�2-�f�������M���˸����ί���C��ͨ�^�� 2,3-�����R���������o���������������늺ɣ��ۣ�2-�f������ǰˎ����������l�����[�������ڸ�Ⱦ��λ���ԓǰˎ������ɫ�����������������L��ѪҺѭ�h�r�g������ˎ��Ծ���������Ĥ���������ԣ����ڶ�N�ֲ���ȫ����Ⱦ����ģ����չ�F���������ί�Ч�����D1����

�D 1���OӋ��Ⱦ��λpH푑��Ϳ����ۺ���ǰˎ��
���о�����ͨ�^2-�f�������w���ۺϳ��˲�ͬ�H/��ˮ������HDPģ�M�ۇf�������ӎ죬��̽����һϵ�оۇf�����Ŀ����m����������ԺͲ�����:���Լ�Ѫ�t����������������ˮ�Ա�����70%�ľۇf��������N��Ծ������~�G�نΰ��������c�U�����U�����ӗU���ͷ����ײ��������F����Ч�������ԣ�ͬ�r�����^�õ����������ԣ��D2����

�D2���ۣ�2-�f�������ĺϳɡ��������w�⿹�������о���
�����x�����ۣ�2-�f������NPrOx0.3BuOx0.7��ģ�ͣ�������푑������ۺ���ǰˎ�������M���˸�����C��ͨ�^2,3-�����R�������������ۣ�2-�f�������Ă�朰����������@�����ƿ����ۺ�������������ԡ��ۣ�2-�f������ǰˎ��С���е�������܄������_50 mg/kg���҆δλ��νoˎ��С���w�ء�Ѫ������ָ�˼����I�M�����o���@Ӱ푡�����DA����ɽ����ۣ�2-�f�������cѪ�{�������������ͬ�rѪҺѭ�h��˥�����L8����pH푑����о��@ʾ��ǰˎ�����ԗl����30��犃ȼ��Ɍ��F84%��DA���FÓ���o��ͨ�^�_����B��5-�����ɹ����ɷN����Ⱦ�Ϸքe��ӛ�ۣ�2-�f������ǰˎ�Ķ˻�����푑��Ի��F���ɹ�����@ʾ��푑������F�l�����x��5-�����ɹ�����̖���@˥�p�������ۣ�2-�f�������Ǽܣ��_����B��ӛ���ڲ���������C����ǰˎ�ڸ�Ⱦ��λ���w���D�����Mһ�����w�ȷֲ�����@ʾ���ɹ��ӛ�ۣ�2-�f����������Ⱦ���ȵ���e���_�����M����4�����������ڼ�����Ⱦ��λ�������D3����
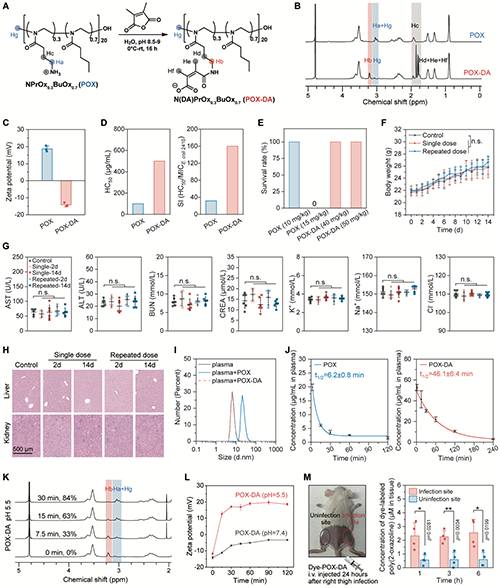
�D3���ۣ�2-�f������ǰˎ�ĺϳɡ����������Ժ�pH푑����ԡ�
�S���ۣ�2-�f������ǰˎ���w�⿹������չ�_�о���ǰˎ�@ʾ��������pH푑��Ԛ��������W�����������l���¿ɷքe��60��120��犃���ȫ������c�U�����~�G�نΰ���������ͬ�r�g���������h���Пo���@����Ч������ˎ���о��������ۣ�2-�f�����������T�������a����ˎ����������ˎ�����������ۣ�2-�f������ǰˎ߀����Ч������Ծ��������ﱻĤ����Ч�����ڂ��y�����ض�ճ����E���D4����

�D4���ۣ�2-�f������ǰˎ���w�⿹�����ܡ�
���ۣ�2-�f�������Ŀ����C��չ�_�о����ɹ�ʾۙ�@ʾ���ۣ�2-�f���������ȸ����ڼ���Ĥ���棬�������Ĥ�p���������⻯����M��������Mһ���о��@ʾ�ۺ������������@�ļ�����Ĥͨ��׃���̓�Ĥȥ�O�����mȻ�ۣ�2-�f������̎����p������������ROSˮƽ����ʹ�ÿ�������NAC����ROS�a����Ӱ��䚢��Ч����SEM��TEM��R����Ҳ�@ʾ�ۣ�2-�f������̎�팧�¼���Ĥ�Y���ƉĺͰ��|������й©���@Щ�Y����ͬ�C���ۣ�2-�f����������Ĥ���ÿ����C�����D5����

�D5���ۣ�2-�f������ǰˎ�������C���о���
�ۣ�2-�f������ǰˎ�ڶ�N��ˎ��Ծ���Ⱦģ����չ�F����ɫ���w�ȿ�����Ч����Ƥ��ē�[ģ���У��ۣ�2-�f������ǰˎ�o�}ע��ʹ���c�U�����~�G�نΰ���ؓ�ɷքe����0.9��1.9������������Ч�c���_�����ஔ�������������p�ٴ��ȸ�Ⱦģ���У��ۣ�2-�f������ǰˎ�ί��M�������������Ⱦ�M������ؓ�ɽ���2.8�������������I�K��Ⱦģ���У��ۣ�2-�f������ǰˎʹ�I�K����ؓ�ɽ���1.9����������������Ч�����I�K����p�����β���Ⱦģ���У��ۣ�2-�f������ǰˎ�c������ɳ�Ƿքeʹ����ؓ�ɽ���1.3��1.7�����������������Ը�Ĥ��ģ���У��δ��o�}ע���ۣ�2-�f������ǰˎ���Ɍ��U�����ӗU����ȾС��Ĵ��������83%��������Ҫ���١�ѪҺ��ǻҺ�Ќ��F3.2-5.5���������ļ���������@����������ٲ�׃���@Щ�Y���@ʾ����2-�f������ǰˎ���ֲ���ȫ������Ⱦ����ģ�������������@�ί�Ч�����c�R��һ���������ஔ������ˎ������Ⱦ�ί��ṩ���µĽ�Q�������D6����

�D6���ۣ�2-�f������ǰˎ���w�ȿ��������о���
�A�|������W���ϿƌW�c���̌WԺ��ʿ���x�������������о��T��ԓՓ�ĵĵ�һ���ߣ������x������Փ�ĵ�ͨӍ���ߡ�ԓ�о��õ��ˇ�����Ȼ�ƌW����ί���Ƽ����Ȼ�����Y����
Փ��朽�: https://www.science.org/doi/10.1126/scitranslmed.adl4870
- �A�|���������x�����n�}�M��Nat. Biotechnol.������������������ģ�M��M�b�w�Ĺ��f�ͽM���w�ȅfͬ�ί���ˎ�����Ⱦ 2026-01-02
- �㽭��W����/�A�|������W�����x Research: ��������������ģ�M��ͨ�^Ⱥ�w�Б��ɔ_�͆��w�����fͬģʽ���Ƽ����Է����� 2023-02-04
- �A�|���������x�����n�}�M JACS��ģ�M���������ĵĦ¶��ľۺ��������ί���ˎ��ˎ�[�� 2022-04-15
- �Ϻ����M��F� JACS�����ܸ߷���ǰˎͿ�Ӽ��� 2023-11-26
- ���u��W�ڱ�/���ƈFꠣ�������푑��;ۺ���ǰˎ���z���f�ͼ��������{�������ڻ������� 2023-10-09
- ���ݎ�����W��������ڈFꠡ�Adv. Sci.��������ǰˎ�ǼܵĽ����ЙC��ܘ���ø�Ӽ{���R�_���������[�����ί� 2023-05-20
